题目内容
【题目】被誉为“太空金属”的钛(Ti),在自然界中主要以金红石(TiO2)的形式存在.由于金红石熔点高,为金属Ti的直接制备带来了困难.在工业上常常采用将其先转化成熔沸点较低的TiCl4后再进行还原的方法.金红石转化成TiCl4的反应方程式如下:
TiO2+2C+2Cl2═TiCl4+2CO
(1)指出该反应的氧化剂 ,氧化产物 ;
(2)用双线桥法标出电子转移;
(3)当有6mol电子转移,则有 mol还原剂被氧化.
【答案】(1)Cl2,CO;(2)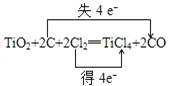 (3)3
(3)3
【解析】
试题分析:(1)根据化学反应,Cl元素的化合价降低,C元素的化合价升高,则Cl2为氧化剂,C为还原剂,CO是氧化产物。
(2)在反应中,C元素的化合价由0升高到+2价,失电子数目是2,Cl元素的化合价由0降低为-1价,得到电子数目共为2,Cl元素守恒,所以氯气前边系数是2,根据电子守恒,碳单质和一氧化碳前边系数都是2,根据钛元素守恒,所以二氧化钛前边系数是1,方程式为:TiO2+2C+2Cl2═TiCl4+2CO,电子转移情况如下: 。
。
(3)根据化学方程式,当消耗2mol碳单质时,转移的电子为4mol,当有6mol电子转移,则有3mol还原剂C被氧化。

练习册系列答案
相关题目