题目内容
【题目】已知常温下某二元酸发生如下电离:H2A=H++HA-;HA-![]() H++A2-(Ka=1×10﹣2)。则下列说法中正确的是( )
H++A2-(Ka=1×10﹣2)。则下列说法中正确的是( )
A. NaHA溶液呈酸性,因为HA-的电离程度大于水解程度
B. 常温下pH=10的Na2A溶液中c(A2-)是c(HA-)的108倍
C. 常温下pH=2的H2A溶液中c(A2-)小于c(HA-)
D. 0.1mol/LH2A溶液中c(A2-)+c(HA-)+c(H2A)=0.1mol/L
【答案】B
【解析】A、该二元酸的一级电离是完全的,故HA-不水解,选项A错误;B、pH=10的Na2A溶液中![]()
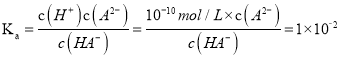 ,
, 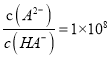 ,选项B正确;C、常温下pH=2的H2A溶液中
,选项B正确;C、常温下pH=2的H2A溶液中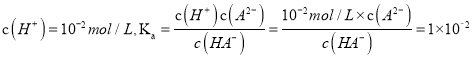 ,则c(A2-)=c(HA-),选项C错误;D、0.1mol/LH2A溶液中不存在H2A分子,选项D错误。答案选B。
,则c(A2-)=c(HA-),选项C错误;D、0.1mol/LH2A溶液中不存在H2A分子,选项D错误。答案选B。

练习册系列答案
相关题目