��Ŀ����
����Ŀ��V��W��X��Y��Z�����ֳ����Ķ���������Ԫ�أ�����W��X��Y��Zԭ�Ӱ뾶��ԭ�������ı仯��ͼ��ʾ��

��֪Y������������Ӧ��ˮ�����������⻯�ﷴӦ�������Σ�Z�ǵؿ��к�������Ԫ�أ�Wԭ�ӵ�������������Neԭ�ӵ��������������1��VΪԭ�Ӻ�����12�����ӵĶ��۽�������2 .4��V���������ᷴӦʱ���ڱ�״���·ų�����2.24L����ش��������⣺
��1��ָ��YԪ�������ڱ��е�λ��_________��
��2��д��W�ļ����ӵĽṹʾ��ͼ_______________��
��3���Ƚ�W����̬�⻯����H2S��HF���ȶ��ԣ���ǿ������____________�����ѧʽ��
��4����W��Y����Ԫ����ɵ�һ�ֻ����ÿ��ԭ���������ﵽ8�����ȶ��ṹ��д���û�����ĵ���ʽ____________��
��5����X��Y��Z����Ԫ����ɵĻ������һ�ֳ����Ļ��ʣ���ԭ�Ӹ�����Ϊ4��2��3��������ʺ��еĻ�ѧ������Ϊ_____________��
��6��V��W��Ԫ������������ˮ���ﷴӦ�Ļ�ѧ����ʽ______________________��
���𰸡� ��2���ڢ�A�� ![]() HF ��HCl��H2S �� ���Ӽ������ۼ� Mg(OH)2+2HClO4��Mg(ClO4)2 + 2H2O
HF ��HCl��H2S �� ���Ӽ������ۼ� Mg(OH)2+2HClO4��Mg(ClO4)2 + 2H2O
��������V��W��X��Y��Z�����ֳ����Ķ�����Ԫ�أ�Y������������Ӧ��ˮ�����������⻯�ﷴӦ�������Σ�Y��N��X��ԭ������С��N����ԭ�Ӱ뾶С��N����XΪHԪ�أ�Z�ǵؿ��к�������Ԫ�أ�Z��O��Wԭ�ӵ�������������Neԭ�ӵ��������������1��W��ԭ��������ԭ�Ӱ뾶�����W��Na��VΪԭ�Ӻ�����12�����ӵĶ��۽�������2.4gV���������ᷴӦʱ���ڱ�״���·ų�����2.24L����������������0.1mol������V����Է���������2.4��0.1��24�����V����������24��12��12����V��Mg��
��1��������������֪��NԪ�������ڱ��е�λ���ǵ�2���ڢ�A�壻��2�������ӵĽṹʾ��ͼΪ![]() ����3���ǽ�������F��Cl��S�����⻯���ȶ�����HF ��HCl��H2S����4����W��Y����Ԫ����ɵ�һ�ֻ����ÿ��ԭ���������ﵽ8�����ȶ��ṹ���û������ǵ����ƣ��������Ӽ�������ʽΪ
����3���ǽ�������F��Cl��S�����⻯���ȶ�����HF ��HCl��H2S����4����W��Y����Ԫ����ɵ�һ�ֻ����ÿ��ԭ���������ﵽ8�����ȶ��ṹ���û������ǵ����ƣ��������Ӽ�������ʽΪ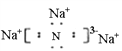 ����5����X��Y��Z����Ԫ����ɵĻ������һ�ֳ����Ļ��ʣ���ԭ�Ӹ�����Ϊ4��2��3��������������泥����еĻ�ѧ������Ϊ���Ӽ����ۼ�����6��þ��Cl��Ԫ������������ˮ���ﷴӦ�Ļ�ѧ����ʽΪMg(OH)2+2HClO4��Mg(ClO4)2 + 2H2O��
����5����X��Y��Z����Ԫ����ɵĻ������һ�ֳ����Ļ��ʣ���ԭ�Ӹ�����Ϊ4��2��3��������������泥����еĻ�ѧ������Ϊ���Ӽ����ۼ�����6��þ��Cl��Ԫ������������ˮ���ﷴӦ�Ļ�ѧ����ʽΪMg(OH)2+2HClO4��Mg(ClO4)2 + 2H2O��

 ѧ���쳵�����ּ��ں�����ҵϵ�д�
ѧ���쳵�����ּ��ں�����ҵϵ�д� ��˼ά������ҵϵ�д�
��˼ά������ҵϵ�д�����Ŀ��
����ͪ����ɫ��dz��ɫ��Һ�壬��ǿ�ҵĴ̼��Գ�ζ���ܶȣ����ˮ=1����0.95���۵㣺-45�����е㣺155�����ܽ�ȣ�100mL H2O����2.4g��31������
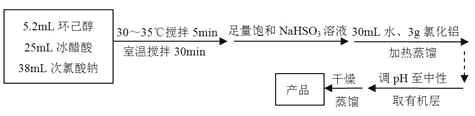
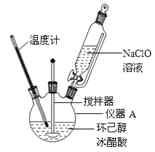
����Ӧ��
�ش��������⣺
��1������A�������� ��
��2���ڷ�Ӧ��ʼ��5min��Ϊ�˽���ϵ�¶�ά����30��35���������ñ�ˮԡ��ȴ�⣬��ȡ�Ĵ�ʩ���� �� ��
��3�����뱥��NaHSO3��Һʱ��������Ҫ��Ӧ�� �������ӷ���ʽ��ʾ����ȷ������ı���NaHSO3��Һ�Ѿ�������ʵ������� ��
��4��Ϊ�����Һ��pH�������ԣ����Լ�����Լ��� ��
A��ϡ���� | B����ˮ̼���� | C��Ũ���� | D���������ƹ��� |
��5������pH������뾫��ʳ�Σ���Ŀ���� ����ȡ�л�����ʱʹ�õ���Ҫ������ ��������ͼ��Ӧ����ĸ����
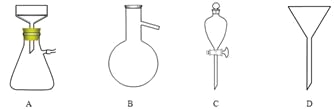
��6��ʵ���������Ż���ʵ��ɰ�������Ҫ��С���Ա�����б�Ҫ��NaClO��Һ�����Ũ�Ƚ���̽��������������һϵ�в�ͬŨ�ȵ�NaClO��Һ�����õζ����궨�����巽���ǣ�����Һ��ȡ10.00mL NaClO��Һ��500mL����ƿ�ж��ݣ�ȡ25.00mL����ƿ�У���������ϡ�����KI���壨����������0.1000mol/L Na2S2O3����Һ�ζ����յ㣨�õ�����Һ��ָʾ����������ƽ��ʵ��ƽ������Na2S2O3����Һ18.00mL����֪I2+2Na2S2O3==2NaI+Na2S4O6 �����NaClO��Һ��Ũ���� ��