题目内容
3.海水提溴的主要反应的离子方程式为Cl2+2Br-=2Cl-+Br2,该反应说明两种单质对应元素的非金属性强弱为Cl>Br(用元素符号填空).分析 海水中溴以离子存在,需要加氯水氧化溴离子,发生卤素单质之间的置换反应,可比较非金属性,以此来解答.
解答 解:海水提溴的主要反应的离子方程式为Cl2+2Br-=2Cl-+Br2,元素单质之间的相互置换反应说明元素非金属性强弱,则非金属性Cl>Br,
故答案为:Cl2+2Br-=2Cl-+Br2;Cl;Br.
点评 本题考查海水提溴,为高频考点,把握发生的反应、非金属性比较方法为解答的关键,侧重分析与应用能力的考查,注意海水提溴的原理,题目难度不大.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
14.氮的固定是几百年来科学家一直研究的课题.
(1)如表列举了不同温度下大气固氮和工业固氮的部分K值.
①分析数据可知:大气固氮反应属于吸热 (填“吸热”或“放热”)反应.
②分析数据可知:人类不适合大规模模拟大气固氮的原因K值小,正向进行的程度小(或转化率低),不适合大规模生产.
③从平衡视角考虑,工业固氮应该选择常温条件,但实际工业生产却选择500℃左右的高温,解释其原因从反应速率角度考虑,高温更好,温度越高平衡逆向进行,但从催化剂活性和反应速率等综合因素考虑选择500℃左右合适
(2)工业固氮反应中,在其他条件相同时,分别测定N2的平衡转化率在不同压强(р1、р2)下随温度变化的曲线,如图所示的图示中,正确的是A (填“A”或“B”);比较р1、р2的大小关系р2>р1.

(3)20世纪末,科学家采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现高温常压下的电化学合成氨,提高了反应物的转化率,其实验简图如C所示,阴极的电极反应式是N2+6e-+6H+=2NH3
(4)近年,又有科学家提出在常温、常压、催化剂等条件下合成氨气的新思路,反应原理为:
2N2(g)+6H2O(1)?4NH3(g)+3O2(g),则其反应热△H=+1530 kJ•mol-1.(已知:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1,2H2(g)+O2(g)?2H2O(l)△H=-571.6kJ•mol-1)
(5)液氨和水类似,也能自离解(电离):NH3+NH3═NH4++NH2-.25℃时,液氨的离子积K=1.0×10-30. 若将NaNH2固体加入液氨中,则所得溶液中不存在的关系式是(设温度保持不变)a(选填编号)
a.c(Na+)=c(NH2-) b.c(NH4+)•c(NH2-)=1.0×10-30 c.c(NH2-)>c(NH4+)
(6)若在液氨中NaNH2和NH4Cl都能完全电离,则用标准NaNH2液氨溶液滴定未知浓度NH4Cl液氨溶液时,反应的离子方程式为NH4++NH2-=2NH3.
(1)如表列举了不同温度下大气固氮和工业固氮的部分K值.
| 反应 | 大气固氮 N2(g)+O2(g)?2NO(g) | 工业固氮 N2(g)+3H2(g)?2NH3(g) | |||
| 温度/℃ | 25 | 2000 | 25 | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 5×108 | 20 | 0.152 |
②分析数据可知:人类不适合大规模模拟大气固氮的原因K值小,正向进行的程度小(或转化率低),不适合大规模生产.
③从平衡视角考虑,工业固氮应该选择常温条件,但实际工业生产却选择500℃左右的高温,解释其原因从反应速率角度考虑,高温更好,温度越高平衡逆向进行,但从催化剂活性和反应速率等综合因素考虑选择500℃左右合适
(2)工业固氮反应中,在其他条件相同时,分别测定N2的平衡转化率在不同压强(р1、р2)下随温度变化的曲线,如图所示的图示中,正确的是A (填“A”或“B”);比较р1、р2的大小关系р2>р1.

(3)20世纪末,科学家采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现高温常压下的电化学合成氨,提高了反应物的转化率,其实验简图如C所示,阴极的电极反应式是N2+6e-+6H+=2NH3
(4)近年,又有科学家提出在常温、常压、催化剂等条件下合成氨气的新思路,反应原理为:
2N2(g)+6H2O(1)?4NH3(g)+3O2(g),则其反应热△H=+1530 kJ•mol-1.(已知:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1,2H2(g)+O2(g)?2H2O(l)△H=-571.6kJ•mol-1)
(5)液氨和水类似,也能自离解(电离):NH3+NH3═NH4++NH2-.25℃时,液氨的离子积K=1.0×10-30. 若将NaNH2固体加入液氨中,则所得溶液中不存在的关系式是(设温度保持不变)a(选填编号)
a.c(Na+)=c(NH2-) b.c(NH4+)•c(NH2-)=1.0×10-30 c.c(NH2-)>c(NH4+)
(6)若在液氨中NaNH2和NH4Cl都能完全电离,则用标准NaNH2液氨溶液滴定未知浓度NH4Cl液氨溶液时,反应的离子方程式为NH4++NH2-=2NH3.
14.下列有关物质的性质和该性质的应用均正确的是( )
| A. | 常温下铝与浓硫酸不发生反应,故常温下可用铝制容器贮运浓硫酸 | |
| B. | 碳酸钠可与盐酸反应,故常用于治疗胃溃疡病人的胃酸过多症 | |
| C. | 氧化铝具有很高的熔点,故可用于制造阻燃剂或耐高温材料 | |
| D. | 二氧化硫、潮湿的氯气均具有漂白性,故其混合物的漂白效果会更好 |
11.关于碱金属的性质叙述错误的是( )
| A. | 还原性随原子电子层数的增加而增加 | |
| B. | 在空气中燃烧的生成物都是过氧化物 | |
| C. | 与水反应的剧烈程度随核电荷数增加而增强 | |
| D. | 最高价氧化物对应水化物的碱性随核电荷数增加而增强 |
18.不能与乙酸反应的物质是( )
| A. | Na | B. | NaOH | C. | Ag | D. | Na2CO3 |
8.下列装置中能构成原电池的是( )
| A. |  | B. |  | C. |  | D. |  |
15.下面的排序不正确的是( )
| A. | 晶体熔点由低到高:CF4<CCl4<CBr4<CI4 | |
| B. | 硬度由大到小:金刚石>碳化硅>晶体硅 | |
| C. | 熔点由高到低:Na>Mg>Al | |
| D. | 晶格能由大到小:NaI>NaBr>NaCl>NaF |
13.下列化学用语正确的是( )
| A. | Cl-的结构示意图: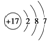 | B. | 甲烷分子的球棍模型 | ||
| C. | 四氯化碳的电子式: | D. | 氯乙烯的结构简式:CH2=CHCl |