题目内容
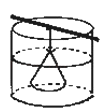
【题目】按如图所示装置进行实验,将液体A逐滴加入到固体B中,下 列叙述不正确的是( )

A. 若A为浓盐酸,B为KMnO4,C中盛品红溶液,则C中溶液褪色
B. 若A为醋酸,B为贝壳,C中盛Na2SiO3,则C中溶液中变浑浊
C. 若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中先产生白色沉淀后沉淀又溶解
D. 实验仪器D可以起到防止溶液倒吸的作用
【答案】C
【解析】
A、浓盐酸和KMnO4反应生成氯气,氯气通入品红溶液,溶于水生成的次氯酸有漂白性,能使品红溶液褪色,故A正确;B、若A为醋酸,B为贝壳,贝壳主要成分是碳酸钙,与醋酸反应会生成二氧化碳气体,Na2SiO3与二氧化碳反应使溶液变浑浊,故B正确;C、浓氨水和生石灰CaO反应生成氨气,氨气溶于水生成氨水,氨水和AlCl3溶液反应生成氢氧化铝沉淀,且氨水是弱碱,不能溶解氢氧化铝,故C错误;D、D为球形结构,可使倒吸的液体受重力作用流下,具有防倒吸作用,故D正确。故选C。

【题目】现有一瓶A和B的混合物,已知甲和乙的某些性质如表所示:( )
物质 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 | 水中的溶解性 |
A | -75 | 66 | 0.93 | 可溶 |
B | -66 | 110 | 0.90 | 可溶 |
据此,将甲和乙互相分离的方法是( )
A.蒸馏法B.升华法C.萃取法D.过滤法
【题目】一定温度下,向10 mL 0.40 mol·L-1 H2O2溶液中加入适量FeCl3溶液,不同时刻测得生成O2的体积(已折算为标准状况)如下表所示:
t / min | 0 | 2 | 4 | 6 |
V(O2) / mL | 0 | 9.9 | 17.2 | 22.4 |
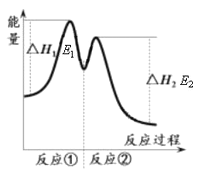
资料显示,反应分两步进行:① 2Fe3++H2O2 == 2Fe2++O2↑+2H+,② H2O2+2Fe2++2H+ == 2H2O+2Fe3+。反应过程中能量变化如下图所示。下列说法错误的是
A. Fe3+的作用是增大过氧化氢的分解速率
B. 反应①是吸热反应、反应②是放热反应
C. 反应2H2O2(aq) == 2H2O(l)+O2(g)的ΔH=E1-E2<0
D. 0~6 min的平均反应速率:v(H2O2)=3.33×10-2 mol·L-1·min-1