题目内容
【题目】t℃时,配制一组c(H2CO3)+c(HCO3-)+c(CO32-)=1.000×10-3mol·L-1的H2CO3与HCl或H2CO3与NaOH的混合溶液,溶液中部分微粒浓度的负对数(-lgc)与pH关系如下图所示。下列说法正确的是( )
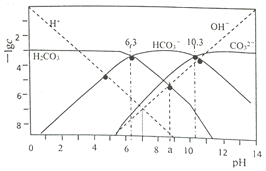
A. pH=6.3的溶液中:c(Na+)>1.000×10-3mol·L-1
B. pH=7的溶液中:c(Na+)>c(H2CO3)>c(CO32-)
C. pH=a的溶液中:c(HCO3-)>c(Na+)>c(H+)>c(CO32-)
D. 25℃时,反应H2CO3+CO32-![]() 2HCO3-的平衡常数为1.0×104
2HCO3-的平衡常数为1.0×104
【答案】BD
【解析】A. pH=6.3的溶液中碳酸略过量:c(H2CO3)+c(HCO3-)+c(CO32-)=1.000×10-3mol·L-1, 故c(Na+)>1.000×10-3mol·L-1,选项A错误;B. pH=7的溶液中:由电荷守恒有c(Na+)+ c(H+)= c(HCO3-)+ 2c(CO32-)+ c(OH-),则c(Na+)> c(CO32-),由图可知c(H2CO3)>c(CO32-),故c(Na+)>c(H2CO3)>c(CO32-),选项B正确;C. pH=a的溶液中,由图中信息可知, c(CO32-)>c(H+),选项C错误;D. 25℃时,pH=6.3时,c(H2CO3)= c(HCO3-),K1=c(H+)=10-6.3,pH=10.3时,c(CO32-)= c(HCO3-),K2=c(H+)=10-10.3,反应H2CO3+CO32-![]() 2HCO3-的平衡常数K=
2HCO3-的平衡常数K=![]() =
=![]() =
=![]() =
=![]() =1.0×104,选项D正确。答案选BD。
=1.0×104,选项D正确。答案选BD。

练习册系列答案
 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案
相关题目