题目内容
【题目】(1)H2O的摩尔质量为:_________ , 36 g 水的物质的量为:_____________如果将这36 水完全电解生成H2和 O2,则所得H2在标况下的体积约为:_________________
(2)1 mol Na2O2中所含阴离子数的个数约为:_________(用NA表示)
(3)将0.5 mol Na2CO3固体加水溶解配成250 mL溶液, c(Na+)=____ mol·L-1。
【答案】18g/mol 2mol 44.8L NA 4
【解析】
(1)H2O的摩尔质量为18g/mol;由n=m/M计算水的物质的量;由V=n×Vm计算;
(2)O22-是原子团;
(3)由c=n/V计算;
(1)H2O的摩尔质量为: 18g/mol, 36 g 水的物质的量为: 36g/18g/mol=2mol;如果将这36 水完全电解生成H2和 O2,则所得H2在标况下的体积约为:V=2mol×22.4L·mol-1=44.8L ;
(2)Na2O2中阴离子为O22-,1 mol Na2O2中所含阴离子数的个数为NA。
(3)将0.5 mol Na2CO3固体加水溶解配成250 mL溶液, c(Na+)=![]() =4mol·L-1。
=4mol·L-1。

【题目】碳、氮等元素及其化合物和人类生产、生活密切相关,请回答下列问题:
(1)氨催化氧化是硝酸工业的基础,生产过程中会发生以下反应:
主反应:![]()
副反应:![]()
①工业上往往采用物料比![]() 在1.7—2.0之间,主要目的是____________。
在1.7—2.0之间,主要目的是____________。
②下表所示是部分化学键的键能参数:
化学键 | N-N | O=O |
键能/kJ· mol-1 | 946 | 497.3 |
则拆开1mol NO中的化学键需要吸收的能量是__________kJ。
(2)在一定温度下,向1L密闭恒容容器中充入l mol NO和一定物质的量的CO,在催化剂作用下发生反应:2NO (g)+2CO (g)![]() 2CO2(g)+N2(g) ΔH>0,NO的物质10 s随反应时间t的变化曲线如图:
2CO2(g)+N2(g) ΔH>0,NO的物质10 s随反应时间t的变化曲线如图:
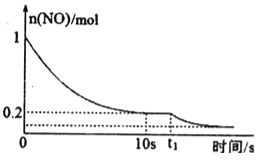
①前10 s内N2的平均生成速率为____。
②已知在t1时刻反应速率加快,则在t1时刻改变的条件可能是____。(填写一种)
(3)在723K时,将0.1mol H2和0.2mol CO2通入抽空的上述密闭容器中,发生如下反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),反应平衡后,水的物质的量分数为0.10。
CO(g)+H2O(g),反应平衡后,水的物质的量分数为0.10。
①CO2 的平衡转化率等于______,反应平衡常数K等于______(保留两位有效数字)。
②再向容器中加入过量的CoO (s)和Co (s),则容器中又会增加如下平衡:CoO (s) +H2 (g)![]() Co (s) +H2O(l)K1;CoO (s) +CO (g)
Co (s) +H2O(l)K1;CoO (s) +CO (g)![]() Co (s) +CO2(g) K2。最后反应平衡时,容器中水的物质的量分数为0. 30,则K1等于____。
Co (s) +CO2(g) K2。最后反应平衡时,容器中水的物质的量分数为0. 30,则K1等于____。