题目内容
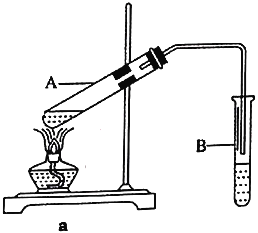
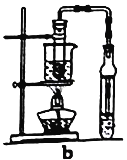
【题目】根据环保要求,在处理有氰电镀废水时,剧毒的CN-离子在催化剂TiO2颗粒作用下,先用NaClO将CN-离子氧化成CNO-(CN-和CNO-中N元素均为-3价),再在酸性条件下继续与NaClO反应生成N2、CO2和Cl2。环保工作人员在密闭系统中用如图装置进行实验,测定CN-被处理的百分率。

现将浓缩后含CN-离子的污水与过量NaClO溶液的混合液共200mL(其中CN-的浓度为0.2mol/L)倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞。回答下列问题:
(1)根据题意,写出相关主要反应的离子方程式:甲中的反应:____,乙中的反应:____。
(2)上述实验是通过测定CO2的量来确定对CN-的处理效果。丙装置中的试剂是____,丁装置的目的是_____;干燥管Ⅱ的作用是_____。
(3)假定上述每一个装置都充分吸收,则利用该装置测得的CN-被处理的百分率与实际值相比_____(填“偏高”或“偏低”),简述可能的原因:_____。
(4)若干燥管Ⅰ中碱石灰增重1.408g,则该实验中测得CN-被处理的百分率为____。
【答案】CN-+ClO-![]() CNO-+Cl- 2CNO-+6ClO-+8H+=N2↑+2CO2↑+3Cl2↑+4H2O 浓硫酸 除去Cl2 防止空气中的CO2、水蒸气进入干燥管I,影响CO2的测量 偏低 前面装置中残留有CO2未被完全吸收 80%
CNO-+Cl- 2CNO-+6ClO-+8H+=N2↑+2CO2↑+3Cl2↑+4H2O 浓硫酸 除去Cl2 防止空气中的CO2、水蒸气进入干燥管I,影响CO2的测量 偏低 前面装置中残留有CO2未被完全吸收 80%
【解析】
含CN-废水放入甲中,在催化剂TiO2颗粒作用下,先用NaClO将CN-离子氧化成CNO-,则自身被还原为Cl-;反应后的溶液进入乙中,在稀硫酸的作用下,NaClO反应生成N2、CO2和Cl2;此时进入丙中的气体为N2、CO2和Cl2,因为干燥管I用于吸收CO2,而N2不能被碱石灰吸收,对CO2含量的测定不产生影响,所以在气体进入干燥管I之前,应将Cl2和水蒸气除尽,铜能与Cl2反应生成FeCl3,所以丙的作用是干燥气体。另外,干燥管Ⅱ的作用是确保干燥管I只吸收CO2,不吸收来自空气中的气体。
(1)根据题意,甲中,NaClO将CN-离子氧化成CNO-,则自身被还原为Cl-,反应的离子方程式为:CN-+ClO-![]() CNO-+Cl-;乙中,NaClO将CNO-转化为N2、CO2和Cl2,反应的离子方程式为:2CNO-+6ClO-+8H+=N2↑+2CO2↑+3Cl2↑+4H2O。答案为:CN-+ClO-
CNO-+Cl-;乙中,NaClO将CNO-转化为N2、CO2和Cl2,反应的离子方程式为:2CNO-+6ClO-+8H+=N2↑+2CO2↑+3Cl2↑+4H2O。答案为:CN-+ClO-![]() CNO-+Cl-;2CNO-+6ClO-+8H+=N2↑+2CO2↑+3Cl2↑+4H2O;
CNO-+Cl-;2CNO-+6ClO-+8H+=N2↑+2CO2↑+3Cl2↑+4H2O;
(2)上述实验是通过测定CO2的量来确定对CN-的处理效果。丙装置中的作用是干燥气体,所加试剂是浓硫酸;据以上分析,丁装置的目的是除去Cl2;干燥管Ⅱ的作用是防止空气中的CO2、水蒸气进入干燥管I,影响CO2的测量。答案为:浓硫酸;除去Cl2;防止空气中的CO2、水蒸气进入干燥管I,影响CO2的测量;
(3)假定上述每一个装置都充分吸收,但装置内残留的气体没有被赶出,被干燥剂I吸收的量偏少,则利用该装置测得的CN-被处理的百分率与实际值相比偏低,简述可能的原因:前面装置中残留有CO2未被完全吸收。答案为:偏低;前面装置中残留有CO2未被完全吸收;
(4)若干燥管Ⅰ中碱石灰增重1.408g,则被吸收的CO2的质量为1.408g,该实验中测得CN-的物质的量为:0.200mL×0.2mol/L=0.04mol,被处理的CN-的物质的量n(CN-)=n(CO2)=![]() =0.032mol,则被处理的CN-的百分率为
=0.032mol,则被处理的CN-的百分率为![]() =80%。答案为:80%。
=80%。答案为:80%。