题目内容
【题目】现有X(g)+Y(g)2Z(g);正反应放热.从反应开始经过t1后达到平衡状态,t2 时由于条件改变,平衡受到破坏,在t3时又达到平衡,据如图回答:从t2→t3的曲线变化是由哪种条件引起的( ) 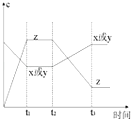
A.增大X或Y的浓度
B.增大压强
C.增大Z的浓度
D.升高温度
【答案】D
【解析】解:A、由图可知,t2秒瞬间浓度都不变化,不可能是增大X或Y的浓度,且若增大了X或Y的浓度,平衡向正反应方向移动,Z的浓度应增大,不符合,故A错误;B、增大了体系压强,平衡不移动,X、Y、Z的浓度应增大,故B错误;
C、若增大Z的浓度,改变条件瞬间Z的浓度应增大,平衡时Z的浓度应大于原平衡,图象与实际不相符,故C错误;
D、该反应放热,升高该反应的温度,平衡逆向移动,X或Y的浓度增大,Z的浓度减小,图象符合,故D正确.
故选D.
【考点精析】解答此题的关键在于理解化学平衡状态本质及特征的相关知识,掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效).

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案【题目】随着学技术的发展和环保要求的不断提高,CO2的捕集利用技术成为研究的重点.完成下列填空:
(1)目前国际空间站处理CO2的一个重要方法是将CO2还原,所涉及的反应方程式为:
CO2(g)+4H2(g) ![]() CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
已知H2的体积分数随温度的升高而增加.若温度从300℃升至400℃,重新达到平衡,判断下列表格中各物理量的变化.(填“增大”、“减小”或“不变”)
v正 | v逆 | 平衡常数K | 转化率α |
(2)相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如表:
[CO2]/molL﹣1 | [H2]/molL﹣1 | [CH4]/molL﹣1 | [H2O]/molL﹣1 | |
平衡Ⅰ | a | b | c | d |
平衡Ⅱ | m | n | x | y |
a、b、c、d与m、n、x、y之间的关系式为 .
(3)碳酸:H2CO3 , Ki1=4.3×10﹣7 , Ki2=5.6×10﹣11
草酸:H2C2O4 , Ki1=5.9×10﹣2 , Ki2=6.4×10﹣5 0.1mol/L Na2CO3溶液的pH0.1mol/L Na2C2O4溶液的pH.(选填“大于”“小于”或“等于”)
等浓度草酸溶液和碳酸溶液中,氢离子浓度较大的是 .
若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是 . (选填编号)
a.[H+]>[HC2O4﹣]>[HCO3﹣]>[CO32﹣]b.[HCO3﹣]>[HC2O4﹣]>[C2O42﹣]>[CO32﹣]
c.[H+]>[HC2O4﹣]>[C2O42﹣]>[CO32﹣]d.[H2CO3]>[HCO3﹣]>[HC2O4﹣]>[CO32﹣].