题目内容
【题目】生活中的有机物种类丰富,在衣食住行等多方面应用广泛,其中乙醇是比较常见的有机物。
(1)乙醇是无色有特殊香味的液体,密度比水_____。
(2)工业上用乙烯与水反应可制得乙醇,该反应的化学方程式为___。(不用写反应条件)
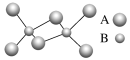
(3)下列属于乙醇的同系物的是___,属于乙醇的同分异构体的是____。(选填编号)
A.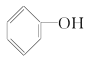 B.
B.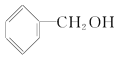 C.CH3CH2—O—CH2CH3
C.CH3CH2—O—CH2CH3
D.CH3OH E.CH3—O—CH3 F.HO—CH2CH2—OH
(4)乙醇能够发生氧化反应:
①乙醇在铜作催化剂的条件下可被氧气氧化,反应的化学方程式为________。
②46g乙醇完全燃烧消耗___mol氧气。
③下列说法正确的是___(选填字母)。
A.乙醇不能和酸性高锰酸钾溶液发生氧化还原反应
B.实验室制乙烯时,温度控制在140℃
C.黄酒中某些微生物将乙醇氧化为乙酸,于是酒就变酸了
D.陈年的酒很香是因为乙醇和乙醇被氧化生成的乙酸发生酯化反应
【答案】小 CH2=CH2+H2O![]() CH3CH2OH D E 2C2H5OH+O2
CH3CH2OH D E 2C2H5OH+O2![]() 2CH3CHO+2H2O 3 CD
2CH3CHO+2H2O 3 CD
【解析】
(1)乙醇密度比水小;
(2)乙烯中含双键可和水发生加成反应生成乙醇;
(3)根据同系物及同分异构体的概念分析;
(4)乙醇含有羟基,可发生催化氧化,可燃烧,可发生取代反应和消去反应,以此解答该题。
(1)乙醇是无色具有特殊香味的密度比水小液体;
(2)乙烯中含双键可和水发生加成反应生成乙醇,反应方程式为:CH2=CH2+H2O![]() CH3CH2OH;
CH3CH2OH;
(3)结构相似,在组成上相差若干个CH2原子团的物质互称同系物,故乙醇的同系物有甲醇,合理选项是D;
分子式相同结构不同的有机物互称同分异构体,乙醇的同分异构体为甲醚,合理选项是E;
(4)①乙醇在铜作催化剂的条件下加热,可被氧气氧化为乙醛,反应的化学方程式为2C2H5OH+O2![]() 2CH3CHO+2H2O;
2CH3CHO+2H2O;
②46 g乙醇的物质的量n(C2H5OH)=46 g÷46 g/mol=1 mol,根据乙醇燃烧的方程式:C2H5OH+3O2![]() 2CO2+3H2O,可知1 mol乙醇完全燃烧消耗3 mol氧气;
2CO2+3H2O,可知1 mol乙醇完全燃烧消耗3 mol氧气;
③A.乙醇含有羟基,能和酸性高锰酸钾溶液发生氧化还原反应使酸性高锰酸钾溶液褪色,A错误;
B.实验室制乙烯时,温度控制在170℃,B错误;
C.黄酒中某些微生物将乙醇氧化为乙酸,乙酸具有酸性,于是酒就变酸了,C正确;
D.陈年的酒很香是由于乙醇和乙醇被氧化生成的乙酸发生酯化反应生成了具有特殊香味的乙酸乙酯,因此而具有香味,D正确;
故合理选项是CD。

 优生乐园系列答案
优生乐园系列答案【题目】下列有机化学反应方程式及反应类型均正确的是
选项 | 化学反应方程式 | 反应类型 |
A | CH3COOH+CH3CH2OH | 酯化反应 |
B | CH4+Cl2 | 置换反应 |
C | CH2=CH2+Br2 CH3CHBr2 | 加成反应 |
D |
| 取代反应 |
A. A B. B C. C D. D
【题目】硫及其化合物有许多用途,相关物质的物理常数如下表所示:
H2S | S8 | FeS2 | SO2 | SO3 | H2SO4 | |
熔点/℃ | -85.5 | 115.2 | >600(分解) | -75.5 | 16.8 | 10.3 |
沸点/℃ | -60.3 | 444.6 | -10.0 | 45.0 | 337.0 |
回答下列问题:
(1)基态Fe原子价层电子的轨道表示式为_________,基态S原子电子占据最高能级的电子云轮廓图为________形。
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是____________。
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为___________。
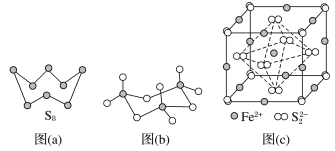
(4)气态三氧化硫以单分子形式存在,其分子的立体构型为____________形,其中共价键的类型有________种;固体三氧化硫中存在如图(b)所示的三聚分子,该分子中S原子的杂化轨道类型为__________。
(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M、阿伏加德罗常数的值为NA,其晶体密度的计算表达式为______g·cm-3。