题目内容
【题目】硝酸是极其重要的化工原料,工业上将产生的NO2在密闭容器中用水多次反复循环吸收制备硝酸。
(1)工业上用水吸收NO2生产HNO3,生成的气体经多次氧化、吸收的循环操作充分转化为硝酸(假定上述过程无其他损失)。试写出上述反应的化学方程式:_______
(2)为了证明NO也可以与氧气和水共同反应生成HNO3,某学生设计了如图所示装置(有关夹持装置已略去)。

①检查装置气密性良好后,为观察到NO气体生成,打开K1,关闭K2,应从U形管的长管口注入稀硝酸至____后,迅速关闭K1,观察到U形管内的现象是______。
②装置Ⅲ中发生反应的化学方程式为__________。
③蘸NaOH溶液的棉花团的作用是____________。
④打开K2,至装置Ⅱ中长玻璃管中的气体呈无色后,打开K3,反应一段时间后,长玻璃管中并未充满液体。设计简单方法检验长玻璃管中的气体是否含NO______。
【答案】(1)4NO2+O2+2H2O=4HNO3(或分成两个方程式写)
(2)①U形管右侧胶塞下沿 U形管左端液面高于右端,铜丝慢慢溶解,产生无色气体,溶液逐渐变蓝(至少答三点)
②2H2O2![]() 2H2O+O2↑
2H2O+O2↑
③吸收氮的氧化物防止污染环境
④再打开K3,若观察到长玻璃管中气体迅速变为红棕色,则证明余气含NO,若无颜色变化,则证明不含NO(其他合理答案也可)
【解析】
解答本题要注意以下两点:(1)根据实验目的和所放置的试剂确定各装置的作用。
(2)三个开关K1、K2、K3的开与关都对实验起着重要作用。

 阅读快车系列答案
阅读快车系列答案【题目】为了探究化学能与热能的转化,某实验小组设计了如图所示的三套实验装置:
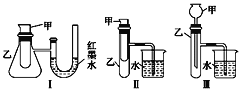
(1)上述3个装置中,不能证明“铜与浓硝 酸反应是吸热反应还是放热反应”的是(不能用手触摸和使用温度计)___________。
(2)某同学选用装置Ⅰ进行实验(实验前U形管里液面左右相平),在甲试管里加入 适量氢氧化钠溶液与稀盐酸,U形管中可观察到的现象是______________,说明该反应属于_____ (填“吸热”或“放热”)反应。
(3)为定量测定(2)中反应的反应热,使50 mL 0.50 mol·L-1盐酸与50 mL0.55 mol·L-1NaOH溶液在简易量热计中进行中和反应.回答下列问题:
①该实验中NaOH的浓度大于HCl的浓度的作用是_________________________。
②实验中若改用60 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液进行反应,与上述实验相比,所求中和热_________ (填“相等”或“不相等”)。
(4)已知一些化学键的键能数据如表所示:
化学键 | C—H | C—F | H—F | F—F |
键能/kJ·mol-1 | 414 | 489 | 565 | 155 |
请根据键能数据估算CH4(g)和F2(g)反应生成CF4(g)和HF(g)的热化学方程式:_______________。