题目内容
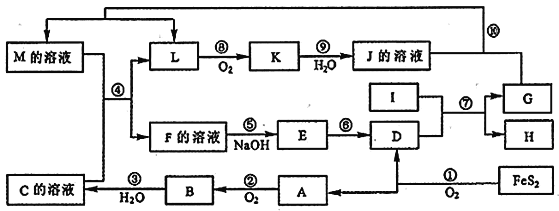
【题目】下图中A~H均为中学化学中常见的物质,A、B、H是气体,它们之间有如下转化关系。(反应中生成的水已略去)
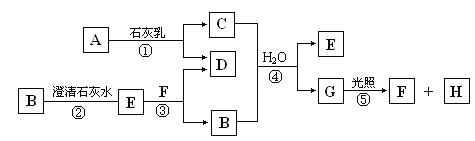
请回答以下问题:
(1)E是______(填化学式)。
(2)C物质在日常生活中可作______剂。
(3)写出反应④ 的化学方程式:____________。
(4)写出实验室制取A气体的化学反应方程式,并用双线桥表示电子转移的方向和数目:_________。
【答案】CaCO3 消毒(或漂白) Ca(ClO)2+CO2+H2O=CaCO3+2HClO 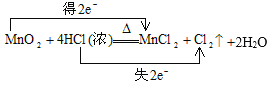
【解析】
B可与澄清石灰水反应生成沉淀,应为CO2,则E为CaCO3,常见的能与石灰水反应的气体还有氯气,则A应为Cl2,由此可知C为Ca(ClO)2,F为HCl,D为CaCl2,G为HClO,H为O2,在实验室中用MnO2与浓盐酸混合加热制取Cl2,根据氧化还原反应中元素化合价升降与电子转移关系用双线桥法表示。
B可与澄清石灰水反应生成沉淀,应为CO2,则E为CaCO3,常见能与石灰水反应的气体还有氯气,则A应为Cl2,由此可知C为Ca(ClO)2,F为HCl,D为CaCl2,G为HClO,H为O2。
(1)由以上分析可知E为CaCO3;
(2)C为Ca(ClO)2,该物质与酸溶液作用可生成HClO,HClO具有强氧化性和漂白性,可用于消毒或漂白;
(3)反应④是Ca(ClO)2与CO2、H2O作用产生HClO,反应的化学方程式为:Ca(ClO)2+CO2 +H2O= CaCO3+2HClO;
(4)在实验室中用MnO2与浓盐酸混合加热制取Cl2,反应方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O。在该反应中,Mn元素化合价由反应前MnO2中的+4价变为反应后MnCl2中的+2价,化合价降低,获得2e-,Cl元素的化合价由反应前HCl中的-1价变为反应后Cl2中的0价,化合价升高,失去2×e-,用双线桥法表示为:
MnCl2+Cl2↑+2H2O。在该反应中,Mn元素化合价由反应前MnO2中的+4价变为反应后MnCl2中的+2价,化合价降低,获得2e-,Cl元素的化合价由反应前HCl中的-1价变为反应后Cl2中的0价,化合价升高,失去2×e-,用双线桥法表示为: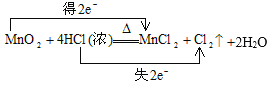 。
。