题目内容
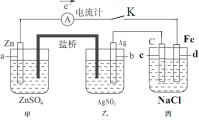
【题目】以多孔铂为电极,在如图装置中分别在两极区通入CH3OH和O2,发生反应产生电流,经测定,电流方向由b到a,下列叙述中正确的是( )

A.负极的电极反应为:2CH3OH+16OH-12e-=2CO32-+12H2O
B.溶液中的阳离子向a极运动
C.A处通入O2
D.b极是该燃料电池的负极
【答案】A
【解析】
A选项,电流方向由b到a,说明a为负极,b为正极,在A处应通入CH3OH,负极即a极的电极反应为:2CH3OH+16OH--12e-=2CO32-+12H2O,故A正确;
B选项,电流方向由b到a,说明a为负极,b为正极,原电池中溶液中的离子是“同性相吸”即阴离子向负极移动,阳离子向正极移动即b极移动,故B错误;
C选项,电流方向由b到a,说明a为负极,b为正极,在A处应通入CH3OH,故C错误;
D选项,电流方向由b到a,说明a为负极,b为正极,故D错误;
综上所述,答案为A。

【题目】砷(![]() )元素广泛的存在于自然界,在周期表中的位置如表。
)元素广泛的存在于自然界,在周期表中的位置如表。
|
| |
|
| |
|
|
完成下列填空:
(1)砷元素最外层电子的排布式为______________。
(2)砷化镓(![]() )和氮化硼(
)和氮化硼(![]() )晶体都具有空间网状结构,硬度大。砷化镓熔点为1230℃,
)晶体都具有空间网状结构,硬度大。砷化镓熔点为1230℃,![]() 的熔点为3000℃,从物质结构角度解释两者熔点存在差异的原因__________。
的熔点为3000℃,从物质结构角度解释两者熔点存在差异的原因__________。
(3)亚砷酸盐(![]() )在碱性条件下与碘单质反应生成砷酸盐(
)在碱性条件下与碘单质反应生成砷酸盐(![]() ),完成反应的离子方程式: ____
),完成反应的离子方程式: ____![]() +I2+_____ ______。该反应是一个可逆反应,说明氧化还原反应的方向和______有关。
+I2+_____ ______。该反应是一个可逆反应,说明氧化还原反应的方向和______有关。
(4)工业上将含有砷酸盐(![]() )的废水转化为粗
)的废水转化为粗![]() 的工业流程如下:
的工业流程如下:
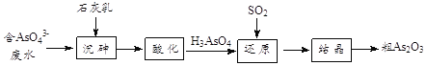
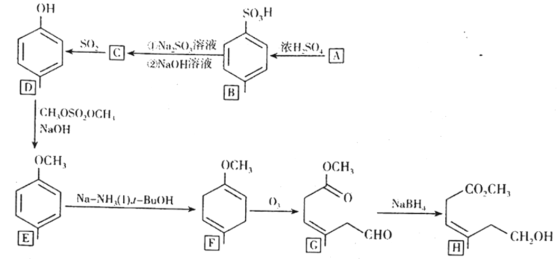
①写出还原过程中砷酸![]() 转化为亚砷酸
转化为亚砷酸![]() 的化学方程式: ___________
的化学方程式: ___________
②“沉砷”是将![]() 转化为
转化为![]() 沉淀,主要反应有:
沉淀,主要反应有:
i.Ca(OH)2(s)Ca2+(aq)+2OH—(aq)+Q
ii.5Ca2++OH—+3![]() Ca5(AsO4)3OH-Q
Ca5(AsO4)3OH-Q
沉砷最佳温度是85℃。用化学平衡原理解释温度高于85℃后,随温度升高沉淀率下降的原因___。