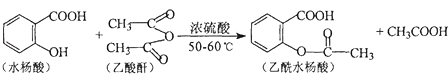
题目内容
【题目】A、B、C、D是原子序数均小于20的四种元素.A与B同主族,且能形成BA2、BA3两种化合物.B、C、D所形成的简单离子电子层结构相同,且B、C、D离子半径依次减小.请回答下列问题:
①D元素在元素周期表中的位置是 .
②A与D所形成的化合物的电子式为 .
③将C单质的水溶液滴加到B与D所形成化合物的水溶液中,其反应的化学方程式为 .
【答案】第四周期第ⅠA族;![]() ;Cl2+S2﹣=2Cl﹣+S↓
;Cl2+S2﹣=2Cl﹣+S↓
【解析】解:A、B、C、D是原子序数均小于20的四种元素.A与B同主族,且能形成BA3型分子,则A为氧元素、B为硫元素;B、C、D所形成的简单离子电子层结构相同,核外电子数为18,且B、C、D离子半径依次减小,则原子序数D>C>B,结合原子序数可知,D为K、C为Cl,①D为K元素,在元素周期表中的位置是:第四周期第ⅠA族,所以答案是:第四周期第ⅠA族;②A与D所形成的化合物为K2O,电子式为 ![]() ,所以答案是:
,所以答案是: ![]() ;③将氯气的水溶液滴加到K2S的水溶液中,硫离子被氧化生成硫,氯气被还还原,同时生成KCl,反应的化学方程式为:Cl2+K2S=2KCl+S↓,所以答案是:Cl2+S2﹣=2Cl﹣+S↓.
;③将氯气的水溶液滴加到K2S的水溶液中,硫离子被氧化生成硫,氯气被还还原,同时生成KCl,反应的化学方程式为:Cl2+K2S=2KCl+S↓,所以答案是:Cl2+S2﹣=2Cl﹣+S↓.

【题目】高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大.以下是某温度下这四种酸在冰醋酸中的电离常数:从表格中判断以下说明不正确的是( )
酸 | HClO4 | H2SO4 | HCl | HNO3 |
Ka | 1.6×10﹣5 | 6.3×10﹣9 | 1.6×10﹣9 | 4.2×10﹣10 |
A.在冰醋酸中,高氯酸的酸性最强
B.水对于这四种酸的强弱没有区分能力,但醋酸可以区分这四种酸的强弱
C.在冰醋酸中1mol/L的高氯酸的电离度约为0.4%
D.在冰醋酸中硫酸的电离方程式为:H2SO4═2H++SO42﹣
【题目】关于以下科技成果,下列说法正确的是( )
A.中国“人造太阳” | B.电磁炮成功装船 | C.“鲲龙”两栖飞机 | D.“墨子”通信卫星 |
利用氘和氚发生化学反应产生上亿度高温 | 电磁炮发射过程中电能转化为机械能 | 飞机大量使用熔点高、硬度大的铝锂合金 | 通讯中使用的光导纤维主要成分是单晶硅 |
A.AB.BC.CD.D