题目内容
下列各组物质互为同系物的是( )
| A.金刚石和石墨 | B. |
| C.CH4和C2H6 | D.16O和18O |
C
试题分析:A.金刚石和石墨是由同种元素组成的不同性质的单质,互为同素异形体,错误;B.
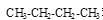
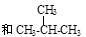 分子式相同,结构不同,是同分异构体,错误;C.CH4和C2H6结构相似,在分子组成上相差一个或若干个CH2原子团,互为同系物,正确;D.16O和18O是由质子数相同而中子数不同的同种元素的不同种原子,互为同位素,错误。
分子式相同,结构不同,是同分异构体,错误;C.CH4和C2H6结构相似,在分子组成上相差一个或若干个CH2原子团,互为同系物,正确;D.16O和18O是由质子数相同而中子数不同的同种元素的不同种原子,互为同位素,错误。
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目