��Ŀ����
����Ŀ���ڻ�ѧ��Ӧ�У�ֻ�м�����������ƽ�������ߵö�ķ�Ӧ����ӷ�����ײʱ�ſ��ܷ�����ѧ��Ӧ����Щ���ӱ���Ϊ����ӡ�ʹ��ͨ���ӱ�ɻ���������ṩ������ȵ������л�ܣ��䵥λͨ����kJmol��1��ʾ��������۲�ͼ1��Ȼ��ش����⡣
��1��ͼ����ʾ��Ӧ��________��������������������������Ӧ��

��2����֪��1mol H��H����1mol I��I��1mol H��I���ֱ���Ҫ���յ�����Ϊ436kJ��151kJ��299kJ������1mol������1mol �ⷴӦ����HI��________�������ų���������������________kJ���������ڻ�ѧ��Ӧ�����У��ǽ�________ת��Ϊ________��
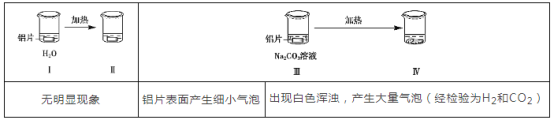
��3��ijʵ��С��ͬѧ������ͼ2��ʵ�飬��̽����ѧ��Ӧ�е������仯��ʵ����������е��¶Ƚ��ͣ��ɴ��ж����������������Ȼ�茶��巴Ӧ��________��������������������������Ӧ��ʵ�����У���С��ͬѧ���ձ��м���5mL 1.0mol/L���ᣬ�ٷ�����ɰֽ��ĥ�����������÷�Ӧ��________��������������������������Ӧ��
���𰸡����� �ų� 11 ��ѧ�� ���� ���� ����
��������
(1)����ͼ�������Ӧ��������������������������Ӧ���ȣ�
(2)�ڷ�ӦH2+I22HI�У�����1molH-H����1molI-I�������յ�����Ϊ��1��436kJ+151kJ=587kJ������2molHI�����γ�2molH-I�����ų�������Ϊ��2��299kJ=598kJ�����յ������٣��ų��������࣬���Ը÷�ӦΪ���ȷ�Ӧ���ų�������Ϊ��598kJ-587kJ=11kJ���ڻ�ѧ��Ӧ�����У�����ѧ��ת��Ϊ���ܣ�
(3)���е��¶Ƚ���˵���÷�Ӧ�����ȷ�Ӧ�����ý����û�������ķ�ӦΪ���ȷ�Ӧ��

����Ŀ�����Ϊ�١����Ԫ�أ���Ԫ�����ڱ��е�λ�����£�
���� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0�� |
1 | �� | �� | ||||||
2 | �� | �� | �� | �� | ||||
3 | �� | �� | �� | �� |
�Իش��������⣺
��1��д��Ԫ�آ۵�����__��
��2���ٺܺ͢�Ԫ���γɵĻ�����Ļ�ѧʽΪ__���õ���ʽ��ʾ���γɹ���Ϊ__��
��3���ߺ͢��Ԫ�ص�����������ˮ����ļ����ǣ�__��__
��4���١��ݡ��ߺ�Ԫ���γɵ�һ�ֻ�����ĵ���ʽ��__���ڸû������мȺ���__�����ֺ���__����