题目内容
【题目】常温下,向0.1 mol/L的硫酸溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验时不同阶段的溶液,下列有关说法中不正确的是
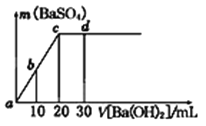
A.溶液的pH:a<b<c<d
B.溶液的导电能力:a>b>d>c
C.c、d溶液呈碱性
D.a、b溶液呈酸性
【答案】C
【解析】
A、a点没有滴入Ba(OH)2溶液,酸性最强,c点沉淀达到最大,说明硫酸全部参加反应,发生的是Ba(OH)2+H2SO4=BaSO4↓+2H2O,d点氢氧化钡过量,因此溶液的pH大小顺序是d>c>b>a,故说法正确;
B、导电能力跟溶液中离子浓度大小有关,离子浓度越大,导电能力越强,c点溶液几乎没有离子,导电能力最弱,因此导电能力a>b>d>c,故说法正确;
C、根据c点反应的方程式,c点为中性溶液,故说法错误;
D、a、b两点硫酸还没中和完,溶液显酸性,故说法正确。
答案选C。

练习册系列答案
相关题目