题目内容
如图所示能够组成原电池,并且产生明显的电流的是( )
A、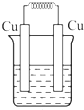 稀硫酸 |
B、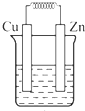 稀硫酸 |
C、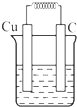 CuSO4 |
D、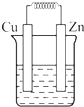 ZnSO4 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:能够组成原电池,并且产生明显的电流,说明该装置符合原电池构成条件,原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应.
解答:
解:A.两个电极材料相同且不能自发的进行氧化还原反应,所以不能构成原电池,导致没有电流产生,故A错误;
B.该装置符合原电池构成条件,所以有电流产生,故B正确;
C.该装置不能自发的进行氧化还原反应,不能构成原电池,没有电流产生,故C错误;
D.该装置不能自发的进行氧化还原反应,不能构成原电池,没有电流产生,故D错误;
故选B.
B.该装置符合原电池构成条件,所以有电流产生,故B正确;
C.该装置不能自发的进行氧化还原反应,不能构成原电池,没有电流产生,故C错误;
D.该装置不能自发的进行氧化还原反应,不能构成原电池,没有电流产生,故D错误;
故选B.
点评:本题考查了原电池原理,明确原电池构成条件是解本题关键,这几个条件必须同时具备,否则不能形成原电池.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a,X、Y是两电极,通过导线与直流电源相连.下列说法不正确的是( )
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a,X、Y是两电极,通过导线与直流电源相连.下列说法不正确的是( )| A、若电镀铜,则Y为铜电极,电解液a可以是硫酸铜或氯化铜溶液 |
| B、若X为铁电极,Y为石墨电极,电解饱和氯化钠溶液一段时间,在两极分别滴加酚酞,X极变红色 |
| C、若X为铂电极,Y为铜电极,a溶液为稀硫酸,经过一段时间后,X极可能析出红色固体 |
| D、若精炼铜,则X用粗铜,Y用精铜 |
下列物质所配成的0.1mol/L溶液中,离子浓度由大到小顺序排列正确的( )
| A、NH4Cl:(Cl-)>(H+)>(NH4+)>(OH-) |
| B、Na2CO3:(Na+)>(CO32-)>(HCO3-)>(OH-)>(H+) |
| C、NaHCO3:(Na+)>(CO32-)>(HCO3-)>(OH-)>(H+) |
| D、(NH4)2SO4:(NH4+)>(SO42-)>(H+)>(OH-) |
 2HI(g)?H2(g)+I2(g)反应过程中能量变化如图所示(图中E1 表示正反应的活化能,E2 表示逆反应的活化能).下列有关叙述正确的是( )
2HI(g)?H2(g)+I2(g)反应过程中能量变化如图所示(图中E1 表示正反应的活化能,E2 表示逆反应的活化能).下列有关叙述正确的是( )| A、该反应为放热反应 |
| B、升高温度,不影响活化分子百分数 |
| C、催化剂能降低该反应的活化能 |
| D、逆反应的活化能等于正反应的活化能 |
加热固体试剂时,不能使用的仪器是( )
| A、试管 | B、烧杯 | C、燃烧匙 | D、坩埚 |
将0.2mol某烷烃完全燃烧后,生成的气体缓缓通过0.5L 2mol/L的NaOH溶液中,生成正盐和酸式盐的物质的量之比为1:3,则该烷烃是( )
| A、乙烷 | B、丙烷 |
| C、2-甲基丙烷 | D、戊烷 |
几种短周期元素的原子半径及主要化合价如表( )
下列叙述错误的是(其中NA表示阿伏加德罗常数的值)
| 元素代号 | X | Y | Z | M | N | P |
| 原子半径/nm | 0.186 | 0.143 | 0.075 | 0.074 | 0.152 | 0.099 |
| 元素的主要化合价 | +1 | +3 | +5、-3 | -2 | +1 | +7、-1 |
| A、X、N元素的金属性:X>N |
| B、Y、M元素形成的离子化合物是工业冶炼Y的原料 |
| C、X单质在M单质中燃烧生成的化合物39g中共含有0.5NA个阴离子 |
| D、标准状况下1L 1mol?L-1的YP3溶液中含有NA个Y3+离子 |
有关如图电化学装置的叙述中,正确的是( )


| A、若X为碳棒,Y为饱和食盐水,K置于N,则铁极上析出氯气 |
| B、若X为铂棒,Y为CuCl2溶液,K置于N,则铁棒质量将增加 |
| C、若X为锌棒,Y为海水,K置于M,形成对铁的外加电流阴极保护 |
| D、若X为铜棒,Y为稀硫酸,K置于M,则正极反应为:Fe-2e→Fe2+ |
“空对空”响尾蛇导弹头部的“红外眼睛”,能分辩出0.001℃的温差变化,它是由热敏陶瓷材料和热释电陶瓷材料做成的.下列叙述中不正确的是( )
| A、“红外眼睛”对热非常敏 |
| B、“红外眼睛”的热目标是敌机发动机或尾部喷口高温区 |
| C、“红外眼睛”的电阻值随温度明显变化 |
| D、“红外眼睛”的工作原理与人眼相同 |