题目内容
(14分)某化学研究性学习小组通过查阅资料,设计了如下图所示的方法来制备KMnO4。
 已知:①3MnO2+KClO3+6KOH
已知:①3MnO2+KClO3+6KOH![]() 3K2MnO4+KCl+3H2O
3K2MnO4+KCl+3H2O
②几种物质的溶解度:
| 温度 | 溶解度/g | ||
| K2CO3 | KOH | KMnO4 | |
| 20℃ | 111 | 112 | 6.38 |
| 60℃ | 127 | 154 | 22.1 |
请回答下列问题:
⑴第一步固体熔融时除三脚架、泥三角、细铁棒、坩埚钳外,还需下列仪器中的 ▲ 。
A.蒸发皿 B.烧杯 C.酒精灯 D.铁坩埚
 ⑵反应Ⅰ中氧化产物与还原产物的物质的量之比为 ▲ ;该反应中可以循环利用的产物是 ▲ 。
⑵反应Ⅰ中氧化产物与还原产物的物质的量之比为 ▲ ;该反应中可以循环利用的产物是 ▲ 。
⑶反应Ⅱ的条件为电解,写出反应Ⅱ的化学方程式 ▲ 。
⑷途径一、二中的操作a、b相同,均包括 ▲ 、过滤等3步。
⑸通过用草酸滴定KMnO4溶液的方法可测定KMnO4粗品的纯度(质量分数)。
①实验时要将草酸晶体(H2C2O4·2H2O)配成标准溶液,则配制100mL1.5mol·L—1的草酸溶液,需要称取草酸晶体的质量为 ▲ 。
②该实验中除草酸晶体的质量外,还需要采集的数据有 ▲ 。
 ⑴CD
⑴CD
⑵2:1 MnO2
⑶2K2MnO4+2H2O![]() 2KOH+2KMnO4+H2↑
2KOH+2KMnO4+H2↑
⑷蒸发浓缩、降温结晶
⑸①18.9g ②滴定时消耗草酸溶液的体积、KMnO4粗品的质量
(每空2分,共14分)

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
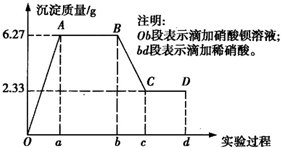 某化学研究性学习小组对某无色水样的成分进行检验,已知该水样中只可能含有K+、Mg2+、Fe3+、Cu2+、Al3+、Ag+、Ca2+、CO
某化学研究性学习小组对某无色水样的成分进行检验,已知该水样中只可能含有K+、Mg2+、Fe3+、Cu2+、Al3+、Ag+、Ca2+、CO
 (2011?泰州一模)某化学研究性学习小组为探究某品牌花生油中不饱和脂肪酸的含量,进行了如下实验:
(2011?泰州一模)某化学研究性学习小组为探究某品牌花生油中不饱和脂肪酸的含量,进行了如下实验:
