��Ŀ����
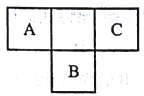
����Ŀ��������Ԫ��A��B��C��Ԫ�����ڱ���������λ����ͼ��ʾ��A��B��C����Ԫ��ԭ�ӵ�������֮��Ϊ32��DԪ��ԭ�ӵ�����������Ϊ�������������2����������˵����ȷ����
A. B����̬�⻯���C����̬�⻯���ȶ�
B. Ԫ��D�γɵ���̬�⻯��һ�������������η���
C. A��B����Ԫ�ص���̬�⻯����������ǵ�����������Ӧ��ˮ�������Ӧ���ҷ�Ӧ������ͬ
D. ����Ԫ�ص�ԭ�Ӱ뾶:B>D>A>C
���𰸡�D
������������ABC����Ԫ�������ڱ��е����λ�ÿ�֪�������A��ԭ��������x����B��x��9��C��x��2����x��x��9��x��2��32�����x��7����A��N��B��S��C��F��DԪ��ԭ�ӵ�����������Ϊ������������2�������D��̼Ԫ�ء�A���ǽ�����Խǿ���⻯����ȶ���Խǿ��F������õķǽ�����HF���ȶ�����ߣ�ѡ��A����ȷ��B��̼Ԫ�ص��⻯����ϩ��ƽ���ͽṹ��ѡ��B����ȷ��A�����������ᷴӦ�ǻ��Ϸ�Ӧ���Ҳ���������ԭ��Ӧ��H2S��Ũ���ᷴӦ��������ԭ��Ӧ����Ӧ���Ͳ�ͬ��ѡ��C����ȷ��D��ͬ����Ԫ�ش�����ԭ�����μ�С��ͬ����Ԫ��ԭ�Ӵ��϶���������������Ԫ�ص�ԭ�Ӱ뾶:B>D>A>C��ѡ��D��ȷ����ѡD��

 ��ʦָ����ĩ��̾�ϵ�д�
��ʦָ����ĩ��̾�ϵ�д� �����ܿ����ϵ�д�
�����ܿ����ϵ�д�