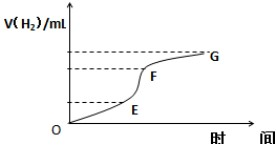
题目内容
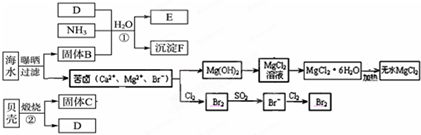
从海水中提取溴的工业流程如图:

(1)以上步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是 .
(2)步骤Ⅱ通入热空气或水蒸气吹出Br2,利用了溴的 .
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(3)以上流程Ⅱ中涉及的离子反应如下,请在下面方框内填入适当的化学计量数及相应物质:
□Br2+□CO32-═□BrO3-+□Br-+□
(4)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏.写出溴与二氧化硫水溶液反应的化学方程式: .
(5)实验室分离溴还可以用溶剂萃取法,下列可以用作溴的萃取剂的是 .
A.乙醇 B.四氯化碳 C.烧碱溶液 D.苯.

(1)以上步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是
(2)步骤Ⅱ通入热空气或水蒸气吹出Br2,利用了溴的
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(3)以上流程Ⅱ中涉及的离子反应如下,请在下面方框内填入适当的化学计量数及相应物质:
□Br2+□CO32-═□BrO3-+□Br-+□
(4)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏.写出溴与二氧化硫水溶液反应的化学方程式:
(5)实验室分离溴还可以用溶剂萃取法,下列可以用作溴的萃取剂的是
A.乙醇 B.四氯化碳 C.烧碱溶液 D.苯.
考点:海水资源及其综合利用
专题:元素及其化合物
分析:(1)步骤Ⅰ中已获得游离态的溴浓度很低,步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是富集溴元素;
(2)溴具有挥发性;
(3)根据元素守恒、原子守恒确定生成物,再结合转移电子守恒、原子守恒配平方程式;
(4)溴具有强氧化性、二氧化硫具有还原性,二者在水溶液中混合易发生氧化还原生成氢溴酸和硫酸;
(5)萃取剂的选取标准:萃取剂和溶质不反应、溶质在萃取剂中的溶解度大于在原溶剂中的溶解度、萃取剂和原溶剂不互溶.
(2)溴具有挥发性;
(3)根据元素守恒、原子守恒确定生成物,再结合转移电子守恒、原子守恒配平方程式;
(4)溴具有强氧化性、二氧化硫具有还原性,二者在水溶液中混合易发生氧化还原生成氢溴酸和硫酸;
(5)萃取剂的选取标准:萃取剂和溶质不反应、溶质在萃取剂中的溶解度大于在原溶剂中的溶解度、萃取剂和原溶剂不互溶.
解答:
解:(1)步骤Ⅰ中已获得游离态的溴浓度很低,如果直接蒸馏,生产成本较高,不利于工业生产,步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是富集溴元素,降低成本,故答案为:富集溴元素;
(2)溴易挥发,步骤Ⅱ通入热空气或水蒸气吹出Br2,就是利用溴的挥发性,故选C;
(3)流程Ⅱ中根据元素守恒知,生成物还有CO2,该反应中Br元素化合价由0价变为-1价、+5价,其最小公倍数是5,再结合原子守恒或电荷守恒得方程式为3Br2+3CO32-═BrO3-+5Br-+3CO2,
故答案为:3;3;1;5;3;CO2;
(4)溴具有强氧化性、二氧化硫具有还原性,二者在水溶液中混合易发生氧化还原生成氢溴酸和硫酸,反应方程式为SO2+Br2+2H2O═2HBr+H2SO4,故答案为:SO2+Br2+2H2O═2HBr+H2SO4;
(5)萃取剂的选取标准:萃取剂和溶质不反应、溶质在萃取剂中的溶解度大于在原溶剂中的溶解度、萃取剂和原溶剂不互溶,
A.乙醇易溶于水,所以不能作萃取剂,故错误;
B.四氯化碳符合萃取剂选取标准,所以能作萃取剂,故正确;
C.烧碱溶液和溴能发生反应,所以不能作萃取剂,故错误;
D.苯符合萃取剂选取标准,所以能作萃取剂,故正确;
故选BD.
(2)溴易挥发,步骤Ⅱ通入热空气或水蒸气吹出Br2,就是利用溴的挥发性,故选C;
(3)流程Ⅱ中根据元素守恒知,生成物还有CO2,该反应中Br元素化合价由0价变为-1价、+5价,其最小公倍数是5,再结合原子守恒或电荷守恒得方程式为3Br2+3CO32-═BrO3-+5Br-+3CO2,
故答案为:3;3;1;5;3;CO2;
(4)溴具有强氧化性、二氧化硫具有还原性,二者在水溶液中混合易发生氧化还原生成氢溴酸和硫酸,反应方程式为SO2+Br2+2H2O═2HBr+H2SO4,故答案为:SO2+Br2+2H2O═2HBr+H2SO4;
(5)萃取剂的选取标准:萃取剂和溶质不反应、溶质在萃取剂中的溶解度大于在原溶剂中的溶解度、萃取剂和原溶剂不互溶,
A.乙醇易溶于水,所以不能作萃取剂,故错误;
B.四氯化碳符合萃取剂选取标准,所以能作萃取剂,故正确;
C.烧碱溶液和溴能发生反应,所以不能作萃取剂,故错误;
D.苯符合萃取剂选取标准,所以能作萃取剂,故正确;
故选BD.
点评:本题考查了海水资源的综合利用,涉及萃取剂的选取、氧化还原反应、方程式的配平等知识点,会从整体上分析流程,知道每一步可能发生的反应及基本操作,再结合基本概念、基本理论解答即可,题目难度中等.

练习册系列答案
相关题目
在CH3COCH3中,中间的碳原子与两边的碳原子成键所用的轨道是( )
| A、SP2-SP2 |
| B、SP3-SP3 |
| C、SP2-SP3 |
| D、SP-SP3 |
重水(D2O)是重要的核工业原料,下列说法错误的是( )
| A、氘(D)原子核外有1个电子 |
| B、1H与D互称同位素 |
| C、H2O与D2O互称同素异形体 |
| D、1H218O与D216O的相对分子质量相同 |
下列叙述中错误的是( )
| A、在通常情况下,甲烷与高锰酸钾等强氧化剂不反应,与强酸、强碱也不反应 |
| B、甲烷燃烧能放出大量的热,所以是一种很好的气体燃料 |
| C、煤矿的矿井要注意通风和严禁烟火,以防爆炸事故的发生 |
| D、点燃甲烷不必像点燃氢气那样事先验纯 |

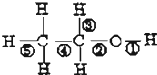 如图是乙醇的结构简式,回答下面的问题:
如图是乙醇的结构简式,回答下面的问题: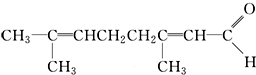
 (溶于水),为了证实该有机物的结构和性质,你认为应先检验
(溶于水),为了证实该有机物的结构和性质,你认为应先检验