��Ŀ����
����Ŀ�������������ʹ�õĽ���֮һ�����������仯�����֪ʶ������������⡣
��1�����ˮ����εμ�1 mol/L FeCl3��Һ����Һ������ĺ��ɫ���÷�ɢϵ������ֱ���ķ�Χ��____________nm��
��2�����ӹ�ҵ��Ҫ��30 %��FeCl3��Һ��ʴ���ھ�Ե���ϵ�ͭƬ����ӡˢ��·�壬��д��FeCl3��Һ��ͭ��Ӧ�����ӷ���ʽ______________________________________��ijͬѧ��FeCl3��ʴͭ��������Һ����ɽ��вⶨ��ȡ����������Һ������KSCN��Һ�ʺ�ɫ������Һ������������������________________��
��3����Ҫ��֤����Һ�к���Fe2������ȷ��ʵ�鷽����________������ĸ�������
A�����Թ��м�����Һ������KSCN��Һ������Ѫ��ɫ��֤������Fe2����
B�����Թ��м�����Һ���������Ը��������Һ������ɫ��֤������Fe2����
C�����Թ��м�����Һ���ȵ���KSCN��Һ���������ٵμ���ˮ������Ѫ��ɫ��֤��ԭ��Һ�к���Fe2��
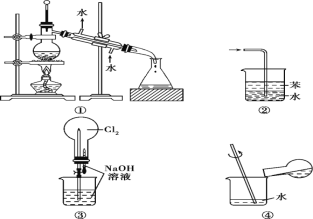
��4�����ӷ�Һ�л���ͭ�������»��FeCl3��Һ���ʵ�鷽�����£�

��д������ʵ�����й����ʵĻ�ѧʽ��A��__________��B��__________��
��д��ͨ�� C�Ļ�ѧ����ʽ_____________________________________________
���𰸡�1��100 2Fe3++Cu=2Fe2++Cu2+ Fe3+��Fe2+��Cu2+ BC Fe HCl 2FeCl2+Cl2=2FeCl3
��������
(1)��Һ������ĺ��ɫ�õ��ķ�ɢϵΪ���壻
(2)FeCl3��Һ��ͭ��Ӧ�����Ȼ�ͭ���Ȼ�������ȡ����������Һ������KSCN��Һ�ʺ�ɫ����һ���������ӣ�
(3)��֤����Һ�к���Fe2+�������仹ԭ�ԣ�ע���ų������Ӷ��������Ӽ���ĸ��ţ�
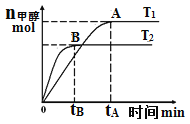
(4)��ʴ��Һ�к����Ȼ�ͭ���Ȼ���������������������Ժ��Ȼ�ͭ��Ӧ���ɽ���ͭ���Ȼ���������AΪFe��������������Һ���Ȼ������������ǽ���ͭ����������ͭ�������ᷴӦ�������������ԣ��������BΪ������Խ�ͭ���룬�õ�����ҺΪ�Ȼ���������Һ�ϲ���ͨ���������ܽ�������������Ϊ���������Դ˽����⡣
(1)���ˮ����εμ�1mol/LFeCl3��Һ����Һ������ĺ��ɫ���÷�ɢϵΪ���壬��֪����ֱ���ķ�Χ��1��100nm��
(2)FeCl3��Һ��ͭ��Ӧ�����Ȼ�ͭ���Ȼ����������ӷ�ӦΪ2Fe3++Cu=2Fe2++Cu2+����ȡ����������Һ������KSCN��Һ�ʺ�ɫ����һ���������ӣ���Cu���㣬��Һ�л���Fe2+��Cu2+��
(3)A�����Թ��м�����Һ������KSCN��Һ������Ѫ��ɫ��֤������Fe3+�����ܼ���Fe2+����A����
B�����Թ��м�����Һ���������Ը��������Һ������ɫ������������ԭ��Ӧ������Fe2+��ԭ�ԣ�֤������Fe2+����B��ȷ��
C�����Թ��м�����Һ�ȵ���KSCN��Һ�����Ժ�ɫ���ٵμ���ˮ����Ѫ��ɫ��֤��ԭ��Һ�к���Fe2����
�ʴ�Ϊ��BC��
(4)��ʴ��Һ�к����Ȼ�ͭ���Ȼ���������������������Ժ��Ȼ�ͭ��Ӧ���ɽ���ͭ���Ȼ���������AΪFe��������������Һ���Ȼ������������ǽ���ͭ����������ͭ�������ᷴӦ�������������ԣ��������BΪ������Խ�ͭ���룬�õ�����ҺΪ�Ȼ���������Һ�ϲ���ͨ���������ܽ�������������Ϊ��������
��������������֪��AΪFe��BΪHCl��
��CΪ������ͨ��C���Ȼ�������Ӧ�����Ȼ���������ʽΪ2FeCl2+Cl2=2FeCl3��

����Ŀ��HClO4��H2SO4��HNO3��HCl����ǿ�ᣬ���ǵ�������ˮ��Һ�в��������ij�¶������������ڱ������еĵ��볣����
�� | HClO4 | H2SO4 | HCl | HNO3 |
Ka | 1.6��10��5 | 6.3��10��9 | 1.6��10��9 | 4.2��10��10 |
����˵���в���ȷ����(����)
A.�ڱ��������������ᶼû����ȫ����
B.�ڱ�������HClO4��������������ǿ����
C.�ڱ�������H2SO4�ĵ��뷽��ʽΪH2SO4===2H����SO![]()
D.ˮ�����������������ǿ����������������������������ǿ��