题目内容
5.下列有关铅蓄电池放电过程叙述正确的是( )| A. | 负极发生的反应为:SO42-+PbO2+2e-+4H+═PbSO4+2H2O | |
| B. | 放电过程中电解液的pH减小 | |
| C. | Pb为负极,反应式为Pb+SO42--2e-═PbSO4 | |
| D. | SO42-向PbO2处移动 |
分析 铅蓄电池放电时,负极是Pb、正极是PbO2,负极反应式为Pb+SO42--2e-═PbSO4,正极反应式为SO42-+PbO2+2e-+4H+═PbSO4+2H2O,放电时,电解质溶液中阳离子向正极移动、阴离子向负极移动,据此分析解答.
解答 解:A.放电时,负极上Pb失电子发生氧化反应,电极反应式为Pb+SO42--2e-═PbSO4,故A错误;
B.根据电池反应式知,放电时,硫酸参加反应,导致溶液中氢离子浓度降低,溶液的pH增大,故B错误;
C.放电时Pb失电子发生氧化反应,则Pb为负极,电极反应式为Pb+SO42--2e-═PbSO4,故C正确;
D.放电时,电解质溶液中阳离子向正极移动、阴离子向负极移动,所以SO42-向负极Pb处移动,故D错误;
故选C.
点评 本题考查原电池和电解池原理,为高频考点,明确得失电子与电极关系、电极反应式的书写是解本题关键,难点是电极反应式的书写,易错点是判断阴阳离子移动方向,题目难度不大.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案
相关题目
13.用NA表示阿斌加德罗常数,下列说法中正确的是( )
| A. | 1mol甲烷中的氢原子被氯原子完全取代,需要2NACl | |
| B. | 1mol•L-1Mg(NO3)溶液中含有NO3-的数目为2NA | |
| C. | 标准状况下.22.4LBr2中所含的分子数为NA | |
| D. | Na2O2与水反应时,每生成0.1 molO2,转移电子的数目为0.2NA |
20.下列反应中,不属于氧化还原反应的是( )
| A. | 2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑ | B. | 3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | ||
| C. | CaCO3+SiO2$\frac{\underline{\;高温\;}}{\;}$CaSiO3+CO2↑ | D. | Zn+H2SO4═ZnSO4+H2↑ |
17.在化学反应3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O中,当有1.5mol铜被氧化时( )
| A. | 有4 mol硝酸被还原 | B. | 有2 mol硝酸被还原 | ||
| C. | 转移6 mol电子 | D. | 转移3 mol电子 |

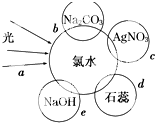 氯气是一种重要的化工原料.
氯气是一种重要的化工原料.