题目内容
据报道,火星和金星大气层中可能存在一种非常特殊的气态化合物。这种化合物会导致温室效应,它的结构式为16O=C=18O。则16O=C=18O
| A.与16O=C=16O互为同素异形体 |
| B.与18O=C=18O有几乎相同的化学性质 |
| C.与Na216O2反应生成的氧气中含有18O |
| D.与等质量的16O=C=16O和18O=C=18O混合气体含有相同的原子个数 |
B
解析试题分析:A.同素异形体是由同种元素组成的不同性质的单质。16O=C=18O与普通的CO2都是化合物。错误。B.18O与16O是同位素原子,其质量不同,物理性质不同,但是化学性质几乎相同,所以与18O=C=18O有几乎相同的化学性质。正确。C.Na2O2与水反应产生的氧气来源与Na2O2。所以与Na216O2反应生成的氧气中含有16O.错误。D、16O=C=16O和18O=C=18O相对分子质量不同,所以等质量时的物质的量不同,根据n=m÷M.可知n不同。由n=N÷NA分子数也就不同,原子数也就不同。错误。
考点:考查同素异形体、同位素的概念的辨析及应用的知识。

 天天练口算系列答案
天天练口算系列答案短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y原子的最外层电子数是其电子层数的3倍。下列说法正确的是( )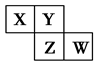
| A.元素Y和元素Z的最高正化合价相同 |
| B.单核阴离子半径的大小顺序为:r(W)>r(Y)>r(Z) |
| C.气态氢化物稳定性:X <Y<Z<W |
| D.元素W的最高价氧化物对应的水化物是强酸 |
卤素单质可以参与很多化学反应, 如:NF3可由NH3和F2在Cu催化剂存在下反应直接得到;反应①: 2NH3+3F2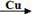 NF3+ 3NH4F
NF3+ 3NH4F
利用“化学蒸气转移法”制备TaS2晶体; 反应②:TaI4(g)+S2(g)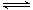 TaS2(s)+2I2(g)+Q kJ,Q>0
TaS2(s)+2I2(g)+Q kJ,Q>0
(1)反应①中:非金属性最强的元素原子核外有_________种不同运动状态的电子;该反应中的某元素的单质可作粮食保护气,则该元素最外层的电子有____________种自旋方向。
(2)反应①中:物质所属的晶体类型有________________________________;
并写出所有原子符合8电子稳定结构的化合物的电子式_______________________。
(3)反应②中:平衡常数表达式K=_____________________,若反应达到平衡后,保持其他条件不变,降低温度,重新达到平衡时 ______________。
| A.平衡常数K增大 | B.S2的浓度减小 | C.I2的质量减小 | D.V(TaI4)逆 增大 |
(5)某同学对反应②又进行研究,他查阅资料,发现硫单质有多种同素异形体,可表示Sx,且在一定条件下可以相互转化,他认为仅增大压强对平衡是有影响的,则TaI4的平衡转化率会____________(填增大或减小),其原因是________________________ 。
下列比较不正确的是
| A.最高价氧化物对应水化物的酸性:H3PO4>H2SO4>HNO3 |
| B.与冷水的反应速率:K>Na>Mg |
| C.热稳定性:HF>HCl>H2S |
| D.离子半径:Cl->F->Na+ |
在11 g由D和18O组成的水中,含中子数为(NA表示阿伏加德罗常数)( )。
| A.NA | B.2NA | C.6NA | D.10NA |
下列叙述正确的是( )
| A.乙酸与丙二酸互为同系物 |
| B.不同元素的原子构成的分子只含极性共价键 |
C.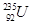 和 和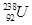 是中子数不同质子数相同的同种核素 是中子数不同质子数相同的同种核素 |
| D.短周期第ⅣA与ⅦA族元素的原子间构成的分子,均满足原子最外层8电子结构 |
下表是元素周期表的一部分,有关说法正确的是( )
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | | | | c | | d | |
| 3 | a | b | | | | e | f |
A.e的氢化物比d的氢化物稳定
B.a、b、e三种元素的原子半径:e>b>a
C.六种元素中,c元素单质的化学性质最活泼
D.c、e、f的最高价氧化物对应的水化物的酸性依次增强
下列元素中价电子排布不正确的是( )
| A.V:3d34s2 | B.Cr:3d44s2 | C.Ar:3s23p6 | D.Ni:3d84s2 |