题目内容
“氢能”将是未来最理想的新能源。
Ⅰ.实验测得,1g氢气燃烧生成液态水时放出142.9kJ热量,则氢气燃烧的热化学方程式为_______。(填序号)
Ⅱ.某化学家根据“原子经济”的思想,设计了如下制备H2的反应步骤
①CaBr2+H2O CaO+2HBr ②2HBr+Hg
CaO+2HBr ②2HBr+Hg HgBr2+H2
HgBr2+H2
③HgBr2+_____ ______________ ④2HgO
______________ ④2HgO 2Hg+O2↑
2Hg+O2↑
请你根据“原子经济”的思想完成上述步骤③的化学方程式:____________。
根据“绿色化学”的思想评估该方法制H2的主要缺点:______________。
Ⅲ.利用核能把水分解制氢气,是目前正在研究的课题。下图是其中的一种流程,其中用了过量的碘。(提示:反应②的产物是O2、SO2和H2O)

完成下列反应的化学方程式:
反应①__________________________;反应②__________________________。
此法制取氢气的最大优点是_______________________________________________。
Ⅳ.氢气通常用生产水煤气的方法制得。其中CO(g)+ H2O(g) CO2(g)+ H2(g); △H<0。
CO2(g)+ H2(g); △H<0。
在850℃时,K=1。
(1)若升高温度到950℃时,达到平衡时K______1(填“大于”、“小于”或“等于”)
(2)850℃时,若向一容积可变的密闭容器中同时充入 1.0 mol CO、3.0molH2O、1.0mol CO2和 x mol H2,则:
①当x=5.0时,上述平衡向___________(填正反应或逆反应)方向进行。
②若要使上述反应开始时向正反应方向进行,则x应满足的条件是__________。
(3)在850℃时,若设x=5.0 mol和x=6.0mol,其它物质的投料不变,当上述反应达到平衡后,测得H2的体积分数分别为a%、b%,则a _______ b(填“大于”、“小于”或“等于”)。
Ⅴ.氢气还原氧化铜所得的红色固体可能是铜与氧化亚铜的混合物,已知Cu2O在酸性溶液中可发生自身氧化还原反应,生成Cu2+和单质铜。
(1)现有8克氧化铜被氢气还原后,得到红色固体6.8克,其中含单质铜与氧化亚铜的物质的量之比是 ;
(2)若将6.8克上述混合物与足量的稀硫酸充分反应后过滤,可得到固体 g;
(3)若将6.8克上述混合物与一定量的浓硝酸充分反应,
①生成标准状况下1.568升的气体(不考虑NO2的溶解,也不考虑NO2与N2O4的转化),则该气体的成分是 ,其物质的量之比是 ;
②把得到的溶液小心蒸发浓缩,把析出的晶体过滤,得晶体23.68g。经分析,原溶液中的Cu2+有20%残留在母液中。求所得晶体的化学式
Ⅰ.实验测得,1g氢气燃烧生成液态水时放出142.9kJ热量,则氢气燃烧的热化学方程式为_______。(填序号)
A.2H2(g)+O2(g)  2H2O(l)△H= -142.9kJ·mol—1 2H2O(l)△H= -142.9kJ·mol—1 |
B.H2(g)+1/2 O2(g)  H2O(l)△H= -285.8kJ·mol—1 H2O(l)△H= -285.8kJ·mol—1 |
C.2H2+O2 2H2O(l)△H= -571.6kJ·mol—1 2H2O(l)△H= -571.6kJ·mol—1 |
D.H2(g)+1/2 O2(g)  H2O(g) △H= -285.8kJ·mol—1 H2O(g) △H= -285.8kJ·mol—1 |
①CaBr2+H2O
 CaO+2HBr ②2HBr+Hg
CaO+2HBr ②2HBr+Hg HgBr2+H2
HgBr2+H2③HgBr2+_____
 ______________ ④2HgO
______________ ④2HgO 2Hg+O2↑
2Hg+O2↑请你根据“原子经济”的思想完成上述步骤③的化学方程式:____________。
根据“绿色化学”的思想评估该方法制H2的主要缺点:______________。
Ⅲ.利用核能把水分解制氢气,是目前正在研究的课题。下图是其中的一种流程,其中用了过量的碘。(提示:反应②的产物是O2、SO2和H2O)

完成下列反应的化学方程式:
反应①__________________________;反应②__________________________。
此法制取氢气的最大优点是_______________________________________________。
Ⅳ.氢气通常用生产水煤气的方法制得。其中CO(g)+ H2O(g)
 CO2(g)+ H2(g); △H<0。
CO2(g)+ H2(g); △H<0。在850℃时,K=1。
(1)若升高温度到950℃时,达到平衡时K______1(填“大于”、“小于”或“等于”)
(2)850℃时,若向一容积可变的密闭容器中同时充入 1.0 mol CO、3.0molH2O、1.0mol CO2和 x mol H2,则:
①当x=5.0时,上述平衡向___________(填正反应或逆反应)方向进行。
②若要使上述反应开始时向正反应方向进行,则x应满足的条件是__________。
(3)在850℃时,若设x=5.0 mol和x=6.0mol,其它物质的投料不变,当上述反应达到平衡后,测得H2的体积分数分别为a%、b%,则a _______ b(填“大于”、“小于”或“等于”)。
Ⅴ.氢气还原氧化铜所得的红色固体可能是铜与氧化亚铜的混合物,已知Cu2O在酸性溶液中可发生自身氧化还原反应,生成Cu2+和单质铜。
(1)现有8克氧化铜被氢气还原后,得到红色固体6.8克,其中含单质铜与氧化亚铜的物质的量之比是 ;
(2)若将6.8克上述混合物与足量的稀硫酸充分反应后过滤,可得到固体 g;
(3)若将6.8克上述混合物与一定量的浓硝酸充分反应,
①生成标准状况下1.568升的气体(不考虑NO2的溶解,也不考虑NO2与N2O4的转化),则该气体的成分是 ,其物质的量之比是 ;
②把得到的溶液小心蒸发浓缩,把析出的晶体过滤,得晶体23.68g。经分析,原溶液中的Cu2+有20%残留在母液中。求所得晶体的化学式
Ⅰ.B (1分)
Ⅱ.HgBr2+CaO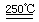 HgO+CaBr2(1分) 循环过程需要很高的能量,且使用重金属汞,会产生污染。(1分)
HgO+CaBr2(1分) 循环过程需要很高的能量,且使用重金属汞,会产生污染。(1分)
Ⅲ.①:SO2+I2+2H2O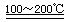 2HI+H2SO4(1分) ②:2H2SO4
2HI+H2SO4(1分) ②:2H2SO4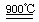 2SO2↑+O2↑+2H2O (1分) SO2和I2可循环使用,无污染。(1分)
2SO2↑+O2↑+2H2O (1分) SO2和I2可循环使用,无污染。(1分)
Ⅳ.(1) 小于(1分) (2) ①逆反应 (1分)② 0≤x<3 (1分) (3) 小于(1分)
Ⅴ.(1)2︰1(1分)(2)4.8克(1分)(3)①NO、NO2(1分) 4︰3 (1分) ②Cu(NO3)2·6H2O(1分)
Ⅱ.HgBr2+CaO
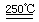 HgO+CaBr2(1分) 循环过程需要很高的能量,且使用重金属汞,会产生污染。(1分)
HgO+CaBr2(1分) 循环过程需要很高的能量,且使用重金属汞,会产生污染。(1分) Ⅲ.①:SO2+I2+2H2O
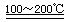 2HI+H2SO4(1分) ②:2H2SO4
2HI+H2SO4(1分) ②:2H2SO4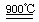 2SO2↑+O2↑+2H2O (1分) SO2和I2可循环使用,无污染。(1分)
2SO2↑+O2↑+2H2O (1分) SO2和I2可循环使用,无污染。(1分) Ⅳ.(1) 小于(1分) (2) ①逆反应 (1分)② 0≤x<3 (1分) (3) 小于(1分)
Ⅴ.(1)2︰1(1分)(2)4.8克(1分)(3)①NO、NO2(1分) 4︰3 (1分) ②Cu(NO3)2·6H2O(1分)
Ⅰ.B氢气燃烧的热化学方程式必须是:1molH2,液态水,放热285.8kJ,所以B正确;
Ⅱ.HgBr2+CaO
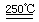 HgO+CaBr2; 循环过程需要很高的能量,且使用重金属汞,会产生污染。生产过程中贯彻落实“绿色化学”的思想。
HgO+CaBr2; 循环过程需要很高的能量,且使用重金属汞,会产生污染。生产过程中贯彻落实“绿色化学”的思想。Ⅲ.①:SO2+I2+2H2O
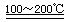 2HI+H2SO4 ;:2H2SO4
2HI+H2SO4 ;:2H2SO4 2SO2↑+O2↑+2H2O ; SO2和I2可循环使用,无污染。
2SO2↑+O2↑+2H2O ; SO2和I2可循环使用,无污染。Ⅳ.(1) 升高温度,平衡逆向移动,平衡常数变小,K小于1(2) ①Qc=1.0×5.0/(1.0×3.0)>1,向逆反应进行,②平衡向正反应方向移动,浓度商小于平衡常数,即
(1×x)/(1×3)<1,解得x<3,故答案为:x<3 0≤x<3 (3)增大一种生产物(氢气)的体积分数,平衡向逆反应方向移动,平衡移动的结果是降低这种增大的幅度,故平衡后氢气的体积分数还是大于原来的,故答案为:小于;
Ⅴ.(1)2︰1(1分)(2)4.8克(1分)(3)①NO、NO2(1分) 4︰3 (1分) ②Cu(NO3)2·6H2O(1分)
(1)n(CuO)=8g/80g·mol-1=0.1mol,氧元素的物质的量=n(CuO)═铜元素的物质的量=0.1mol;固体由CuO生成Cu和Cu2O,减少的质量为氧元素的质量,即8g-6.8g=1.2g,减少的氧元素的物质的量=1.2g/16g·mol-1=0.075mol,所以Cu2O中氧元素的物质的量=0.1mol-0.075mol=0.025mol,所以n(Cu2O)=0.025mol,根据铜元素守恒得n(Cu)=0.1mol-2×0.025mol=0.05mol,所以单质铜与氧化亚铜的物质的量之比是2:1.
故答案为:2:1.
(2)n(Cu)=0.1mol-2×0.025mol=0.05mol,所以m(Cu)=0.05mol×64g·mol-1=3.2g,
氧化亚铜的质量=6.8g-3.2g=3.6g.
氧化亚铜和稀硫酸反应,铜和稀硫酸不反应,设氧化亚铜和稀硫酸反应生成铜的质量为x.
氧化亚铜和稀硫酸反应的方程式为:
Cu2O+H2SO4=CuSO4+Cu+H2O
144g 64g
3.6g x
x=1.6g
所以可得到固体的质量=3.2g+1.6g=4.8克
故答案为:4.8克.
(3)①通过②分析知,6.8克的铜和氧化亚铜的混合物与硝酸反应相当于4.8克的铜与硝酸反应.
设铜与硝酸反应全部生成二氧化氮,二氧化氮的体积为:
Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O
64g 44.8L
4.8g 3.36L
设铜与硝酸反应全部生成一氧化氮,一氧化氮的体积为:
3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
192g 44.8L
4.8g 1.12L
1.12L<1.568l<3.36L,所以该气体是二氧化氮和一氧化氮的混合物.
设生成一氧化氮的物质的量为ymol,生成二氧化氮的物质的量为zmol.
3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
192g 2mol
96yg ymol
Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O
64g 2mol
32zg zmol
y+z=1.568L/22.4L·mol-1
96y+32z=4.8
y=0.04
z=0.03
所以一氧化氮和二氧化氮的物质的量之比为4:3.
故答案为:NO、NO2; 4:3.
②根据铜元素守恒知,氧化铜中的铜全部转化为硝酸铜中的铜离子,为0.1mol,原溶液中的Cu2+有20%残留在母液中,所以晶体中铜离子的物质的量为0.08mol,根据化学式知,晶体中硝酸铜的物质的量=铜离子的物质的量=0.08mol,
m(Cu(NO3)2)=0.08mol×188g·mol-1=15.04g<23.68g,所以晶体中有水,水的物质的量="(23.68g-15.04g)/" 18g·mol-1=0.48mol,硝酸铜与水的物质的量之比=0.08mol:0.48mol=1:6,所以其化学式为Cu(NO3)2·6H2O.
故答案为Cu(NO3)2·6H2O.

练习册系列答案
相关题目
 TiCl4
TiCl4 Ti
Ti 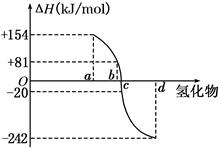

 列叙述中正确的是( )
列叙述中正确的是( )