题目内容
【题目】下列有关说法不正确的是
A. 可用电渗析法进行海水淡化
B. 乙烯与氧气在银催化作用下只生成环氧乙烷(![]() ),该反应符合绿色化学原子经济性要求
),该反应符合绿色化学原子经济性要求
C. 向某溶液中滴入盐酸酸化的氯化钡溶液出现白色沉淀,证明该溶液中一定含有SO42-
D. 酒是陈的香,原因之一是储存过程中生成了有香味的酯
【答案】C
【解析】
A.电渗析法是一种利用离子交换膜进行海水淡化的方法,故A说法正确;
B.乙烯与氧气在银催化作用下只生成环氧乙烷,原子利用率为100%,符合绿色化学原子经济性要求,故B说法正确;
C.向某溶液中滴入盐酸酸化的氯化钡溶液出现白色沉淀,也有可能是AgCl的白色沉淀,不一定含有SO42-,故C说法错误;
D.酒贮存久了其中的乙醇会被氧化成乙酸,两者发生酯化反应而生成了乙酸乙酯,故D说法正确;
答案选C。

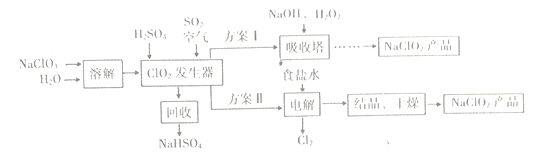
【题目】某工厂的电镀污泥中含有铜、铁等金属化合物。为实现资源的回收利用并有效防止环境污染,设计如下工艺流程:

沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
开始沉淀的pH | 2.3 | 7.6 | 4.4 |
完全沉淀的pH | 3.2 | 9.7 | 6.4 |
(1)酸浸后加入H2O2的目的是_________________。
(2)向CuSO4溶液中加入一定量的NaCl、Na2SO3,可以生成白色的CuCl沉淀,写出该反应的离子方程式____________________。
(3)为保证产品的纯度,调节pH的范围为___________,调pH值可以选用(填字母)_______。
a.Cu(OH)2 b.H2SO4 c.NH3H2O d.Na2CO3 e.CuO
(4)煮沸硫酸铜溶液的原因是____________。
(5)CuCl产品中CuCI的质量分数大于96.50%为国家合格标准。称取所制备的CuCl样品0.2500g置于一定量的0.5mol/LFeCl3溶液中,待样品完全溶解后,加水20mL,用0.1000mol/L的Ce(SO4)2溶液滴定,到达终点时消耗Ce(SO4)2溶液24.80mL。有关的化学反应为Fe3++CuCl=Fe2++Cu2++Cl-,Ce4++Fe2+=Fe3++Ce3+。则CuCl产品中CuCl的质量分数为_____。
(6)已知Fe(OH)3能与次氯酸钾碱性溶液发生反应生成具有强氧化性的高铁酸钾(K2FeO4),高铁酸钾可作为新型多功能水处理剂的原因是___________________。