题目内容
【题目】从煤和石油中可以提炼出化工原料A和B,A是一种果实催熟剂,它的产量用来衡量一个国家的石油化工发展水平.B是一种比水轻的油状液体,B仅由碳氢两种元素组成,碳元素与氢元素的质量比为12:1,B的相对分子质量为78.回答下列问题:
(1)A的电子式 ______________ ,A的结构简式 _______________ .
(2)与A相邻的同系物C使溴的四氯化碳溶液褪色的化学反应方程式 ______________________,反应类型_______________。
(3)在碘水中加入B振荡静置后的现象_________________________
(4)B与浓H2SO4与浓HNO3在50-60℃反应的化学反应方程式 ________________________,反应类型______________________。
(5)等质量的A、B完全燃烧时消耗O2的物质的量______(填“A>B”或“A<B”或“A=B”)。
【答案】(1)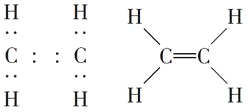
(2)CH2=CH—CH3+Br2―→CH2Br—CHBr—CH3加成反应
(3)下层无色,上层紫红色
(4)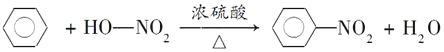 取代反应
取代反应
(5)A>B
【解析】
试题A是一种果实催熟剂,它的产量用来衡量一个国家的石油化工发展水平,则A为CH2=CH2,B是一种比水轻的油状液体,B仅由碳氢两种元素组成,碳元素与氢元素的质量比为12:1,则原子个数之比为1:1,若符合CnH2n-6,B的相对分子质量为78,则B为12n+2n-6=78,解得n=6,所以B为苯。
(1)根据上述分析,A为乙烯,电子式为![]() ,结构简式为CH2=CH2。
,结构简式为CH2=CH2。
(2)A相邻的同系物C为CH2=CHCH3,使溴的CCl4溶液水褪色发生加成反应,该反应为CH3CH=CH2+Br2→CH2BrCHBrCH3,反应类型为加成反应。
(3)碘水中加入苯发生萃取,苯的密度比水的小,则苯在上层,观察到分层 ,下层几乎无色,上层紫红色。
(4)B与浓H2SO4与浓HNO3在50-60℃反应的化学反应方程式为C6H6+HO-NO2![]() C6H5NO2+H2O,该反应属于取代反应。
C6H5NO2+H2O,该反应属于取代反应。
(5)A为乙烯,B为苯,设A、B的质量均为m,由CxHy消耗x+y/4氧气可知,乙烯消耗氧气为m÷28×3= 3m/28,苯消耗氧气为m÷78×7.5=5m/52,则等质量的A、B完全燃烧时消耗O2的物质的量A>B。



