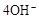题目内容
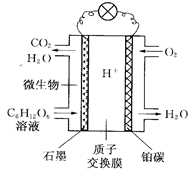
氢氧燃料电池已用于航天飞机。以稀硫酸溶液为电解质溶液的这种电池在使用时的电极反应如下:
负极:2H2—4e—= 4H+; 正极: O2+4e—+4H+ =2H2O
据此作出判断,下列说法中正确的是
负极:2H2—4e—= 4H+; 正极: O2+4e—+4H+ =2H2O
据此作出判断,下列说法中正确的是
| A.O2在正极发生氧化反应 | B.供电时的总反应为:2H2+O2=2H2O |
| C.氢氧燃料电池是把电能转化为化学能 | D.燃料电池的能量转化率可达100% |
B
试题分析:原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。据此可知,氢气在负极通入,氧气在正极通入,选项A不正确,B正确。原电池把化学能转化为电能,C不正确。燃料电池的能量转化率也达不到100%,D不正确,答案选B。
点评:该题是高考中的常见题型,属于中等难度的试题。该题的关键是明确原电池的工作原理,特别是电极名称的判断、电极反应式的书写等。有利于激发学生的学习兴趣,增强学生的学习自信心。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目

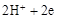 →
→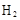 ↑
↑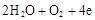 →
→