��Ŀ����
����Ŀ����һ���¶��£���2molA��2molB���������������ݻ�Ϊ2L��ij�ܱ������У��������·�Ӧ��3A(g)+B(g)![]() xC(g)+2D(g)��2minĩ��Ӧ�ﵽƽ��״̬����ʱ���D��C��Ũ�Ⱦ�Ϊ0.4mol/L������д���пհף�
xC(g)+2D(g)��2minĩ��Ӧ�ﵽƽ��״̬����ʱ���D��C��Ũ�Ⱦ�Ϊ0.4mol/L������д���пհף�
(1)xֵ����_____________��
(2)A��ת����Ϊ_______________��
(3)����D�ķ�Ӧ����Ϊ_____________��
(4)�������Ӧ��ϵ��ѹǿ����ƽ����ϵ��C���������� _________������С�䣩��
(5)�ڴ��¶��£��û�ѧ��Ӧ��ƽ�ⳣ��k=__________
���𰸡�x=2 60% 0.2 mol/(L��min) ���� K= 0.5
��������
(1)ƽ��ʱC��D��Ũ��Ϊ0.4mol/L����n(C)=n(D)=0.4mol/L��2L=0.8mol�����n(D)�������ʵ���֮�ȵ��ڻ�ѧ������֮�ȼ���x��
(2)����ƽ��ʱn(D)���ɷ���ʽ��֪�μӷ�Ӧ��n(A)���ٸ���ת���ʶ������A��ת���ʣ�
(3)����v(D)=![]() ���㷴Ӧ���ʣ�
���㷴Ӧ���ʣ�
(4)����Ӧǰ����������ʵ������䣬����ѹǿ��ƽ�ⲻ�ƶ���ƽ����ϵ��C�������������䣻����Ӧǰ����������ʵ����仯������ѹǿƽ�����������ʵ�����С�ķ����ƶ�����������������䣬�ݴ��жϣ�
(5)ƽ�ⳣ��ָָ��һ���¶��£����淴Ӧ�ﵽƽ��ʱ��������Ũ�ȵĻ�ѧ���������ݵij˻����Ը���Ӧ��Ũ�ȵĻ�ѧ���������ݵij˻����õı�ֵ��
(1)ƽ��ʱC��Ũ��Ϊ0.4mol/L����n(C)=n(D)=0.4mol/L��2L=0.8mol���������ʷ�����ѧ��Ӧʱ�仯�����ʵ���֮�ȵ��ڻ�ѧ������֮�ȣ�����0.8mol��0.8mol=x��2�����x=2��
(2)ƽ��ʱn(D)=0.8mol���ɷ���ʽ��֪�μӷ�Ӧ��n(A)=![]() n(D)=
n(D)=![]() ��0.8mol=1.2mol������A��ת����Ϊ
��0.8mol=1.2mol������A��ת����Ϊ![]() ��100%=60%��
��100%=60%��
(3)v(D)=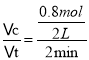 =0.2mol/(Lmin)��
=0.2mol/(Lmin)��
(4)�÷�Ӧ�Ƿ�Ӧǰ����������ʵ�������ķ�Ӧ����������ѹǿ����ѧƽ�ⲻ�ƶ������ƽ����ϵ��C�������������䣻
(5)�ڷ�Ӧ��ʼʱc(A)=c(B)=2mol��2L=1mol/L��c(C)=c(D)=0����Ӧ�ﵽƽ��ʱ��c(C)=c(D)=0.4mol/L���������ʷ�Ӧ��ϵ��֪��Ӧ���ĵ�A��Ũ����0.6mol/L��B��Ũ����0.2mol/L������ƽ��ʱA��B��Ũ�ȷֱ���c(A)=1mol/L-0.6mol/L=0.4mol/L��c(B)=1mol/L-0.2mol/L=0.8mol/L�����Ը÷�Ӧ�Ļ�ѧƽ�ⳣ��K=![]() =0.5��
=0.5��