题目内容
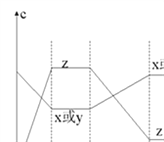
【题目】现有X(g)+Y(g) ![]() 2Z(g);正反应放热。从反应开始经过t1后达到平衡状态,t2时由于条件改变,平衡受到破坏,在t3时又达到平衡,据图回答:从t2→t3的曲线变化是由哪种条件引起的
2Z(g);正反应放热。从反应开始经过t1后达到平衡状态,t2时由于条件改变,平衡受到破坏,在t3时又达到平衡,据图回答:从t2→t3的曲线变化是由哪种条件引起的
A. 增大X或Y的浓度 B. 增大压强
C. 增大Z的浓度 D. 升高温度
【答案】D
【解析】A.由图可知,t2秒瞬间浓度都不变化,不可能是增大X或Y的浓度,且若增大了X或Y的浓度,平衡向正反应方向移动,Z的浓度应增大,不符合,故A错误;
B.增大了体系压强,平衡不移动,X、Y、Z的浓度应增大,故B错误;
C.若增大Z的浓度,改变条件瞬间Z的浓度应增大,平衡时Z的浓度应大于原平衡,图象与实际不相符,故C错误;
D.该反应放热,升高该反应的温度,平衡逆向移动,X或Y的浓度增大,Z的浓度减小,图象符合,故D正确.故选D.

练习册系列答案
相关题目