题目内容
【题目】环之间共用一个碳原子的化合物称为螺环化合物。下列关于螺[4,4]王烷(![]() )的说法错误的是
)的说法错误的是
A. 与环壬烯互为同分异构体 B. 二氯代物有12种(不含立体异构)
C. 所有碳原子不可能都处于同一平面 D. 螺环烷的分子式通式为CnH2n-2
【答案】B
【解析】
A、分子式相同结构不同的化合物互为同分异构体;
B、根据分子中氢原子的种类判断;
C、根据饱和碳原子的结构特点判断;
D、根据烃中碳碳键及环的结构判断分子通式。
A、螺[4,4]王烷(![]() )的分子式为C9H16,环壬烯的分子式也是C9H16,结构不同,互为同分异构体, 选项A正确;
)的分子式为C9H16,环壬烯的分子式也是C9H16,结构不同,互为同分异构体, 选项A正确;
B、分子中的8个氢原子完全相同,二氯代物中可以取代同一个碳原子上的氢原子有1,1-二氯螺[4,4]王烷、2,2-二氯螺[4,4]王烷2种;也可以是相邻碳原子上或者不相邻的碳原子上,有一个氯原子取代在1位则有7种,有一个氯取代在2位的有2种,故总共有11种同分异构体, 选项B错误;
C、由于分子中4个碳原子均是饱和碳原子,而与饱和碳原子相连的4个原子一定构成四面体,所以分子中所有碳原子不可能均处在同一平面上, 选项C正确;
D、螺环烷中含有两个环,则分子式通式为CnH2n-2, 选项D正确。
答案选C。

【题目】I:已知:反应aA(g)+bB(g) ![]() cC(g),某温度下,在 2 L 的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
cC(g),某温度下,在 2 L 的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
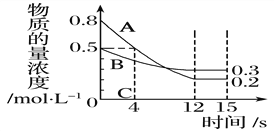
(1)经测定前4 s内v(C)=0.05 mol·L-1·s-1,则该反应的化学方程式为_______________________
(2)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经同一段时间后,测得三个容器中的反应速率分别为甲:v(A)=0.3 mol·L-1·s-1; 乙:v(B)=0.12 mol·L-1·s-1; 丙:v(C)=9.6 mol·L-1·min-1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为__________________(用甲、乙、丙表示)。
Ⅱ: 某学生为了探究锌与盐酸反应过程中的速率变化,他在100 mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气(气体体积已折合成标准状况),实验记录如表(累计值):
时间/min | 1 | 2 | 3 | 4 | 5 | 6 |
氢气体积/mL | 50 | 120 | 224 | 392 | 472 | 502 |
(3)哪一时间段反应速率最大__(填0~1、1~2、2~3、3~4、4~5、5~6 min,下同),原因是_______________________________________________________
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液,你认为可行的是__________(填字母)
A.CH3COONa B.NaNO3溶液 C.KCl溶液 D.Na2CO3溶液
Ⅲ:(5)下列说法可以证明H2(g)+I2(g)![]() 2HI(g)已达平衡状态的是______________________
2HI(g)已达平衡状态的是______________________
A.单位时间内生成n mol H2的同时,生成n mol HI
B.一个H—H键断裂的同时有两个H—I键断裂
C.温度和体积一定时,混合气体颜色不再变化
D.反应速率v(H2)=v(I2)=![]() v(HI)
v(HI)
E.温度和体积一定时,容器内压强不再变化
F.温度和体积一定时,混合气体的密度不再变化