题目内容
【题目】下列结论错误的是:
![]() 微粒半径:
微粒半径:![]()
![]() 氢化物的稳定性:
氢化物的稳定性:![]()
③离子的还原性:![]()
④氧化性:![]()
![]() 酸性:
酸性:![]()
⑥非金属性:![]()
A. 只有![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
【答案】B
【解析】
①离子核外电子层数越多,离子半径越大;当离子核外电子层结构相同时,元素的核电荷数越大,离子半径越小,所以离子半径:S2->Cl->K+>Al3+,①错误;
②元素的非金属性越强,其相应的氢化物的稳定性就越强。元素的非金属性:F>Cl>S>P>Si,所以氢化物的稳定性:![]() ,②正确;
,②正确;
③单质的氧化性越强,则离子还原性越弱。由于氧化性Cl2>Br2>I2>S,所以还原性S2->I->Br->Cl-,③错误;
④同一主族的元素,原子序数越大,单质的氧化性越强;同一周期的元素原子序数越大,单质的氧化性越强,所以氧化性:![]() ,④正确;
,④正确;
⑤元素的非金属性越强,其最高价含氧酸的酸性越强,HClO是弱酸,酸性比H2CO3还弱,因此酸性:![]() ,⑤正确;
,⑤正确;
⑥同一周期元素,原子序数越大,元素的非金属性越强,同一主族的元素,原子核外电子层数越多,元素的非金属性越弱,所以元素的非金属性:![]() ,⑥正确;
,⑥正确;
故说法错误的是①③,则选项B符合题意。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下列离子方程式的书写及评价均合理的是( )
选项 | 离子方程式 | 评价 |
A | 将2 mol Cl2通入含1 mol FeI2的溶液中: 2Fe2++2I-+2Cl2===2Fe3++4Cl-+I2 | 正确;Cl2过量,可将Fe2+、I-均氧化 |
B | Ba(HCO3)2溶液与足量的NaOH溶液反应: Ba2++HCO3-+OH-===BaCO3↓+H2O | 正确;酸式盐与碱反应生成正盐和水 |
C | 过量SO2通入NaClO溶液中: SO2+H2O+ClO-===HClO+HSO3- | 正确;说明酸性:H2SO3强于HClO |
D | 1 mol/L的NaAlO2溶液和2.5 mol/L的HCl溶液等体积混合: 2AlO2-+5H+===Al3++Al(OH)3↓+H2O | 正确;第一步反应和第二步反应消耗的H+的物质的量之比为2∶3 |
A. A B. B C. C D. D
【题目】根据下列短周期元素性质的数据判断,下列说法正确的是![]()
![]()
|
|
|
|
|
|
|
| |
原子半径 |
|
|
|
|
|
|
|
|
最高价或最低价 |
|
|
|
|
|
|
|
|
A. 元素④⑤形成的化合物是离子化合物
B. 元素⑦位于第二周期第VA族
C. 元素①③形成的化合物具有两性
D. 元素③的最高价氧化物对应水化物的碱性最强
【题目】为确定试样Fe2O3、Cu、Fe混合物中铜的质量分数,某同学取质量为ag的试样进行下列实验,所得气体数据在标准状况下测得,所涉及的过程如下:
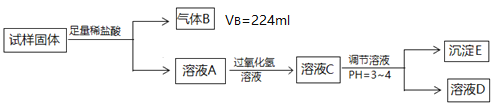
注:已知:Fe3+、Fe2+、Cu2+转化为相应的氢氧化物,开始沉淀和沉淀完全时的pH如下表:
氢氧化物 | Fe3+ | Fe2+ | Cu2+ |
开始沉淀PH | 2.5 | 7.0 | 4.7 |
完全沉淀PH | 3.7 | 9.0 | 6.7 |
下列说法不正确的是
A. 气体B为氢气
B. 溶液A中所含的阳离子可能是H+ 、 Fe3+ 、 Fe2+、 Cu2+
C. 加入过氧化氢溶液时发生的反应:2Fe2++H2O2+2H+=2Fe3++2H2O
D. 若沉淀E经洗涤、烘干、灼烧后得到固体mg,则试样中Cu的质量分数=(a-0.56)/a×100%


