题目内容
1.与甲烷的分子结构相同的物质是( )| A. | CH3Cl | B. | CCl4 | C. | CH2Cl2 | D. | CHCl3 |
分析 甲烷分子中四个H原子为相同的,甲烷形成的是正四面体结构,据此解答即可.
解答 解:甲烷为正四面体结构,
A、CH3Cl相当于甲烷中的1个H被1个Cl原子取代生成的,为四面体结构,不是正四面体结构,故A错误;
B、CCl4相当于甲烷中的4个H被4个Cl原子取代生成的,是正四面体结构,故B正确;
C、CH2Cl2相当于甲烷中的2个H被2个Cl原子取代生成的,为四面体结构,不是正四面体结构,故C错误;
D、CHCl3相当于甲烷中的3个H被3个Cl原子取代生成的,为四面体结构,不是正四面体结构,故D错误,故选B.
点评 本题主要考查的是甲烷的结构以及其氯代物的结构特点判断,比较甲烷中为四个相同的H,其余为Cl取代H的位置,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.甲乙两种非金属,能说明甲比乙的非金属性强的是( )
①甲比乙容易与H2化合;②甲的气态氢化物比乙的气态氢化物稳定;③甲的氧化物对应的水化物的酸性比乙的氧化物对应的水化物酸性强;④与某金属反应时甲原子得电子数目比乙的多;⑤甲的单质熔沸点比乙的低.
①甲比乙容易与H2化合;②甲的气态氢化物比乙的气态氢化物稳定;③甲的氧化物对应的水化物的酸性比乙的氧化物对应的水化物酸性强;④与某金属反应时甲原子得电子数目比乙的多;⑤甲的单质熔沸点比乙的低.
| A. | ①②③ | B. | 只有⑤ | C. | ①②③④⑤ | D. | ①② |
12.现有三种元素的基态原子的电子排布式如下:
①3s23p4;②1s22s22p63s23p3;③1s22s22p5.则上述三种原子的第一电离能大小关系正确的是( )
①3s23p4;②1s22s22p63s23p3;③1s22s22p5.则上述三种原子的第一电离能大小关系正确的是( )
| A. | ②>①>③ | B. | ③>①>② | C. | ③>②>① | D. | ①>②>③ |
9.能发生消去反应,且生成物中存在同分异构体的是( )
| A. | 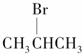 | B. |  | C. |  | D. | CH3Cl |
16.几种短周期元素的原子半径及主要化合价见下表
根据表中信息,判断以下说法正确的是( )
| 元素符号 | X | Y | Z | R | T |
| 原子半径(nm) | 0.160 | 0.080 | 0.102 | 0.143 | 0.074 |
| 主要化合价 | +2 | +2 | -2,+4,+6 | +3 | -2 |
| A. | 单质与稀硫酸反应的速率快慢:R>X>Y | |
| B. | 离子半径:T2->X2+ | |
| C. | 元素最高价氧化物的水化物的碱性:X>R>Y | |
| D. | 单质与氢气化合的难易程度:Z>T |
10.草酸(H2C2O4)是一种重要的有机化工原料.为探究草酸的性质,某化学研究性学习小组查阅了有关资料,有关物质的部分性质如下表:
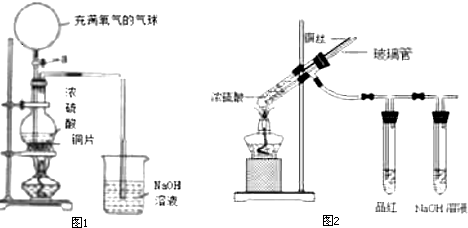
【实验一】根据下图提供的仪器和试剂(可重复使用),设计实验证明草酸受热分解的产物中含有CO2和CO(部分夹持仪器和加热装置省略).
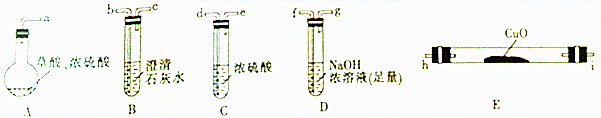
(1)用字母表示接口的正确连接顺序:a→b→c→f→g→d→e→h→i→b→c(部分装置可重复使用).
(2)用上图提供的仪器和试剂做实验时,装置B中出现白色浑浊,也不能说明一定有CO2,请你提出改进意见:在A与B之间添加一个盛水的洗气瓶,除去草酸蒸气(或在烧瓶上连接冷凝管).
(3)利用改进后的装置进行实验时,要先加热A(填“A”“B”“C”“D”或“E”,下同)装置,后加热E装置.
【实验二】利用H2C2O4溶液和酸性KMnO4溶液反应来探究“条件对化学反应速率的影响”.
(4)实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所需的时间来判断反应的快慢.该小组设计了如下方案.
①已知反应后H2C2O4转化为CO2逸出,KMnO4转化为MnSO4,为了观察到紫色褪去,H2C2O4与KMnO4初始的物质的量需要满足的关系为n(H2C2O4):n(KMnO4)≥2.5(或5:2).
②探究温度对化学反应速率影响的实验编号是Ⅱ和Ⅲ;探究反应物浓度对化学反应速率影响的实验编号是I和Ⅱ.
【实验三】H2C2O4溶液浓度的测定.
某同学取一定量草酸晶体配置成100mL溶液,取25.00mL溶液于锥形瓶中,然后用0.10mol•L-1的KMnO4标准溶液滴定该溶液,到达滴定终点时共消耗KMnO4标准溶液24.00mL.
(5)①KMnO4标准溶液应用酸式(填“酸式”或“碱式”)滴定管盛装,滴定终点时的现象是溶液变为紫红色且30s内不变色.
②该同学配制的H2C2O4溶液的物质的量浓度为0.24mol•L-1.
| 物质 | 熔点/℃ | 化学性质 |
| H2C2O4 | 189.5℃ | 二元弱酸,有毒,具有腐蚀性,易溶于水,100℃开始升华,157℃时开始分解,与浓硫酸混合加热会产生CO2、CO和H2O.草酸钙和草酸氢钙均为白色不溶物 |

(1)用字母表示接口的正确连接顺序:a→b→c→f→g→d→e→h→i→b→c(部分装置可重复使用).
(2)用上图提供的仪器和试剂做实验时,装置B中出现白色浑浊,也不能说明一定有CO2,请你提出改进意见:在A与B之间添加一个盛水的洗气瓶,除去草酸蒸气(或在烧瓶上连接冷凝管).
(3)利用改进后的装置进行实验时,要先加热A(填“A”“B”“C”“D”或“E”,下同)装置,后加热E装置.
【实验二】利用H2C2O4溶液和酸性KMnO4溶液反应来探究“条件对化学反应速率的影响”.
(4)实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所需的时间来判断反应的快慢.该小组设计了如下方案.
| 编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度/℃ | ||
| 浓度/mol•L-1 | 体积/mL | 浓度/mol•L-1 | 体积/mL | ||
| Ⅰ | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
| Ⅱ | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| Ⅲ | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
②探究温度对化学反应速率影响的实验编号是Ⅱ和Ⅲ;探究反应物浓度对化学反应速率影响的实验编号是I和Ⅱ.
【实验三】H2C2O4溶液浓度的测定.
某同学取一定量草酸晶体配置成100mL溶液,取25.00mL溶液于锥形瓶中,然后用0.10mol•L-1的KMnO4标准溶液滴定该溶液,到达滴定终点时共消耗KMnO4标准溶液24.00mL.
(5)①KMnO4标准溶液应用酸式(填“酸式”或“碱式”)滴定管盛装,滴定终点时的现象是溶液变为紫红色且30s内不变色.
②该同学配制的H2C2O4溶液的物质的量浓度为0.24mol•L-1.
11.金属钛(Ti)被称为未来“钢铁”,也称为“太空金属”.对钛元素的同位素${\;}_{22}^{46}$Ti、${\;}_{22}^{47}$Ti、${\;}_{22}^{48}$Ti、${\;}_{22}^{49}$Ti、${\;}_{22}^{50}$Ti,下列说法中不正确的是( )
| A. | 上述同位素中,Ti原子核中的中子数不可能为30 | |
| B. | 题述中包括5种钛原子,即钛元素的5种核素 | |
| C. | 根据题意可求得钛元素的平均相对原子质量为48 | |
| D. | 钛元素属过渡金属元素 |
 (1)BCl3的分子构型sp2.第一电离能介于B、N之间的第二周期元素有3种.写出与BCl3结构相同的一种等电子体NO3-或CO32-(写离子).
(1)BCl3的分子构型sp2.第一电离能介于B、N之间的第二周期元素有3种.写出与BCl3结构相同的一种等电子体NO3-或CO32-(写离子).