��Ŀ����
����Ŀ���������ƴ�������Ⱦ�Ϻ��л��ϳɹ�ҵ����ľм�Ʊ��������Ƶ�������ͼ1�� 
��֪���������У����Ʒ�ӦҺ���¶���55��60�������·�������Ҫ��ӦΪ��C6H12O6+12HNO3�T3H2C2O4+9NO2��+3NO��+9H2O
��1�����ܹ����У������������ �� ������ɺ�����Һ����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӵõ���ɫ��״���������ƣ�
��2��ʵ����ģ�����������չ��̵�װ����ͼ2��ʾ��Aװ������Ʒ�ӦҺ���¶Ȳ�����60���ԭ������Bװ�������Ʊ��������ƣ�����ʢ�ŵ���Һ��������ĸ���� 
a��NaCl��Һb��Na2CO3��Һc��NaNO3��Һ
��3����ҵ�������չ����������NO��NO2�����ʵ����Ƚӽ�1��1������NO����n��NO2����1��1����ᵼ������n��NO����n��NO2����1��1��ʹ��Ʒ�л��е�����Ϊ ��
��4����֪NaNO2�ܰ����������µ�Fe2+������ͬʱ����һ���ж������壬��д���÷�Ӧ�����ӷ���ʽ�� ��
��5����֪����NaNO2�������ԣ��������������ܰ�I������ΪI2��S2O32�����ܰ�I2��ԭΪI�� �� ��NaNO2Ҳ�л�ԭ�ԣ���ʹ����KMnO4��Һ��ɫ��Ϊ�ⶨ��ƷNaNO2�Ĵ��ȣ��벹������ʵ�鷽����ȷ����������NaNO2��Ʒ������ƿ�У�������ˮ�ܽ⣬ �� ʵ���пɹ�ѡ����Լ���ϡ���ᡢc1 molL��1 KI��Һ��������Һ��c2 molL��1 Na2S2O3��Һ��c3 molL��1����KMnO4��Һ��
���𰸡�
��1��������ʹ��ά��ˮ���Ϊ������
��2���¶ȹ��ᵼ��HNO3�ֽ⣬����NaNO2�IJ��ʣ�b
��3���ŷ�������NO�������ߣ�NaNO3
��4��NO2��+2H++Fe2+=NO��+Fe3++H2O
��5��Ȼ����c3mol?L��1����KMnO4��Һ�ζ�����Һ����ɫǡ�ñ�Ϊdz��ɫ���Ұ�����ڲ���ɫ���������ظ����ϲ���2��3��
���������⣺��1�����ܹ����У�����������Ǵ��������Դ��ǣ�������ʹ��ά��ˮ���Ϊ�����ǣ���2�������ֽ⣬��Aװ������Ʒ�ӦҺ���¶Ȳ�����60���ԭ�����¶ȹ��ᵼ������ķֽ⣬ʹNaNO2���ʽ��ͣ���Ӧ�в�����NO2��NO��̼������Һ���ռ�ת��Ϊ�������ƣ����Դ��ǣ��¶ȹ��ᵼ������ķֽ⣬ʹNaNO2���ʽ��ͣ�b����3��NO��NO2�����ʵ�����=1��1ʱǡ�ÿ��Կ��������ᣬ�������NO����n��NO2����1��1����ᵼ���ŷ�������NO�������ߣ���n��NO����n��NO2����1��1ʱNO2���������ֻ���������ƣ�����ʹ��Ʒ�л��е�����ΪNaNO3 �� ���Դ��ǣ��ŷ�������NO�������ߣ�NaNO3��4����֪NaNO2�ܰ����������µ�Fe2+������˵����Ԫ�صĻ��ϼ۽��ͣ�ͬʱ����һ���ж������壬��˸�������NO�����Ը÷�Ӧ�����ӷ���ʽΪNO2��+2H++Fe2+=NO��+Fe3++H2O�����Դ��ǣ�NO2��+2H++Fe2+=NO��+Fe3++H2O����5������NaNO2�л�ԭ�ԣ���ʹ����KMnO4��Һ��ɫ�����Կ���ͨ��������ԭ�ζ��ⶨ�䴿�ȣ����ʵ�鷽�����Ϊ��ȷ����������NaNO2��Ʒ������ƿ�У�������ˮ�ܽ⣬Ȼ����c3molL��1����KMnO4��Һ�ζ�����Һ����ɫǡ�ñ�Ϊdz��ɫ���Ұ�����ڲ���ɫ���������ظ����ϲ���2��3�Σ� ���Դ��ǣ�Ȼ����c3molL��1����KMnO4��Һ�ζ�����Һ����ɫǡ�ñ�Ϊdz��ɫ���Ұ�����ڲ���ɫ���������ظ����ϲ���2��3�Σ�

 �Ķ��쳵ϵ�д�
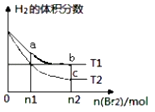
�Ķ��쳵ϵ�д�����Ŀ���¶�ΪTʱ����2.0L�����ܱ������г���1.0mol PCl5����ӦPCl5��g��PCl3��g��+Cl2��g������һ��ʱ���ﵽƽ�⣮��Ӧ�����вⶨ�IJ������ݼ�����
t/s | 0 | 50 | 150 | 250 | 350 |
n��PCl3��/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
����˵����ȷ���ǣ� ��
A.��Ӧ��ǰ50 s��ƽ������v��PCl3��=0.003 2 molL��1s��1
B.���������������䣻�����¶ȣ�ƽ��ʱc��PCl3��=0.11 molL��1����Ӧ�ġ�H��0
C.��ͬ�¶��£���ʼʱ�������г���1.0 mol PCl5��0.20 mol PCl3��0.20 mol Cl2����Ӧ�ﵽƽ��ǰv��������v���棩
D.��ͬ�¶��£���ʼʱ�������г���2.0 mol PCl3��2.0 mol Cl2���ﵽƽ��ʱ��PCl3��ת����С��80%
����Ŀ��ij��Һ�п��ܺ��е��������±���ʾ��
���ܴ������е������� | H+��Mg2+��Al3+��NH4+��Fe3+ |
���ܴ������е������� | Cl-��NO3-��SO42-��CO32-��AlO2- |
Ϊ̽����ɷ֣�������̽��ʵ�顣ȡһ��������Һ����������μ�������������Һ���������������ʵ���(n)���������������Һ�������V���Ĺ�ϵ��ͼ��ʾ��
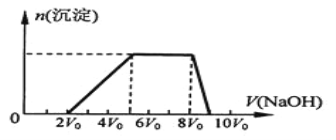
��1������Һ��һ�������ڵ���������_____________
��2������Һ��һ�������ڵ���������_____________
��3������Һ�к��е����������Ӧ�����ʵ���Ũ��֮��Ϊ____________________________
��4��д���������ٹ����з�����Ӧ�����ӷ���ʽ____________________________