题目内容
17.NO2压缩成N2O4可作火箭燃料中的氧化剂,也可制备硝化试剂N2O5等.(1)火箭燃料燃烧反应如下:
2N2H4(l)+N2O4(l)═3N2(g)+4H2O(l)△H,若1.00g N2H4(l)与足量N2O4(l)完全反应生成N2(g)和H2O(l),放出19.10kJ的热量.则反应△H=-1222.4kJ•mol-1
(2)在2L密闭容器内,投入一定量NO2,发生下列反应:2NO2(g)?2NO(g)+O2(g).
在三种不同的条件下进行实验,NO2的浓度随时间的变化如图1所示.
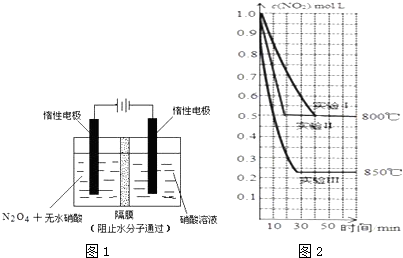
请回答下列问题:
①不能说明该反应已达到平衡状态的是a(填字母).
a.2v正(NO2)=v逆(O2) b.NO2浓度不变 c.气体总压不变 d.NO的体积分数保持不变
②下列说法正确的是ad(填字母).
a.800℃时,该反应的平衡常数为0.25
b.实验Ⅱ和实验Ⅰ相比,可能隐含的条件是:实验Ⅰ使 用了效率更高的催化剂
c.该反应是放热反应
d.实验Ⅰ条件下反应的平衡常数等于实验Ⅱ条件下反应 的平衡常数
e.该反应的△S>0,故该反应一定是自发反应
③实验Ⅱ从反应开始到刚达到平衡时,v(NO)=0.0125mol•L-1•min-1;若再向该2L密闭容器中通 入1mol NO2、1mol NO、0.5mol O2,则NO2的转化率将减小(填“增大”、“减小”或“不变”)
(3)利用NO2或N2O4可制备N2O5,原理如图2所示.N2O5在电解池的阳极区生成,其电极反应为N2O4+2HNO3-2e-=2N2O5+2H+.
分析 (1)计算2molN2H4反应放出的热量,可得该反应的△H,反应放热,焓变符号为“-”,单位为kJ/mol;
(2)①a.不同物质表示的正逆速率之比等于化学计量数之比,反应到达平衡;
b.平衡时c(NO2)浓度不变是平衡标志;
c.随反应进行,压强增大,气体总压不变说明到达平衡;
d.平衡时各组分的含量不变;
②a.计算平衡时各组分的浓度,代入平衡常数表达式K=$\frac{{c}^{2}(NO)c({O}_{2})}{{c}^{2}(N{O}_{2})}$计算;
b.实验Ⅱ和实验Ⅰ相比,反应速率加快,平衡时二氧化氮的浓度相等,不影响平衡移动;
c.升高温度,平衡时二氧化氮的浓度减小,说明升高温度平衡向正反应移动;
d.平衡常数随温度变化;
e.升高温度平衡向正反应移动,正反应为吸热反应,当△G=△H-T△S<0,反应自发进行;
③根据v=$\frac{△c}{△t}$计算v(NO2),利用速率之比等于化学计量数之比计算v(O2);
计算浓度商Qc,与平衡常数比较判断反应方向,若Qc=K,处于平衡状态,Qc<K,向正反应进行,Qc>K,向逆反应进行;
(3)利用NO2或N2O4可制备N2O5,N元素发生氧化反应,则N2O5在电解池的阳极区生成,由图可知,阳极上是 N2O4失去电子,在HNO3条件下生成N2O5,根据电荷守恒可知有H+生成.
解答 解:(1)1.00g N2H4完全反应放出19.14kJ的热量,则2molN2H4反应放出的热量为19.10kJ×$\frac{2mol×32g/mol}{1g}$=1222.4kJ,故该反应的△H=-1222.4kJ/mol,
故答案为:-1222.4;
(2)①a.v正(NO2)=2v逆(O2),则v逆(NO2)=v正(NO2),反应处于平衡状态,2v正(NO2)=v逆(O2),不能说明反应达到平衡状态,故a选;
b.平衡时c(NO2浓度不变,反应达到平衡状态,故b不选;
c.随反应进行,压强增大,气体总压不变说明到达平衡,故c不选;
d.生成物NO的体积分数不变,说明反应到达平衡,故d不选,
故选:a;
②a.800℃时,平衡时二氧化氮的浓度为0.5mol/L,则:
2NO2(g)?2NO(g)+O2(g)
起始量(mol/L):1 0 0
变化量(mol/L):0.5 0.5 0.25
平衡量(mol/L):0.5 0.5 0.25
800℃时平衡常数K=$\frac{{c}^{2}(NO)c({O}_{2})}{{c}^{2}(N{O}_{2})}$=$\frac{0.{5}^{2}×0.25}{0.{5}^{2}}$=0.25,故a正确;
b.实验Ⅱ和实验Ⅰ相比,反应速率加快,平衡时二氧化氮的浓度相等,不影响平衡移动,不能是升高温度或增大压强,实验Ⅱ可能使用了效率更高的催化剂,故b错误;
c.升高温度,平衡时二氧化氮的浓度减小,说明升高温度平衡向正反应移动,而升高温度平衡向吸热反应移动,故正反应为吸热反应,故c错误;
d.平衡常数随温度变化,实验Ⅰ和实验Ⅱ温度相同,实验Ⅰ条件下反应的平衡常数等于实验Ⅱ条件下反应的平衡常数,故d正确;
e.升高温度平衡向正反应移动,正反应为吸热反应,△H>0,正反应为熵减的反应,△S<0,而△G=△H-T△S>0反应不能自发进行,故f错误,
故选:ad;
③v(NO2)=$\frac{1mol/L-0.5mol/L}{20min}$=0.025mol/(L.min),速率之比等于化学计量数之比,v(NO)=v(NO2)=0.025mol/(L.min),
若再向该2L密闭容器中通 入1mol NO2、1mol NO、0.5mol O2,浓度商Qc═0.5>K=0.25,反应向逆反应进行,NO2转化率减小,
故答案为:0.0125mol/(L.min);减小;
(3)利用NO2或N2O4可制备N2O5,N元素发生氧化反应,则N2O5在电解池的阳极区生成,由图可知,阳极上是 N2O4失去电子,在HNO3条件下生成N2O5,根据电荷守恒可知有H+生成,电极反应式为:N2O4+2HNO3-2e-=2N2O5+2H+,
故答案为:阳极;N2O4+2HNO3-2e-=2N2O5+2H+.
点评 本题考查化学平衡计算、平衡状态判断、平衡常数计算与应用、反应热计算、电解原理等,是对学生综合能力的考查,难度中等.

| A. | SiO2 | B. | Br2 | C. | Na2O | D. | Na |
| A. |  | B. |  | C. |  | D. |  |
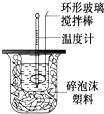 利用下图装置测定中和热的实验步骤如下:
利用下图装置测定中和热的实验步骤如下:①用量筒量取50mL 0.25mol/L硫酸倒入小烧杯中,测出硫酸温度;
②用另一量筒量取50mL 0.55mol/L NaOH溶液,并用另一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液最高温度.回答下列问题:
(1)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热数值为57.3kJ/mol):NaOH(aq)+$\frac{1}{2}$H2SO4(aq)=$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3kJ/mol.
(2)倒入NaOH溶液的正确操作是:C. (从下列选项中选出).
A.沿玻璃棒缓慢倒入 B.分三次少量倒入C.一次迅速倒入
(3)实验数据如下表:①请填写下表中的空白:
| 温度 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 | |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 | |
| 4 | 26.4 | 26.2 | 26.3 | 29.8 | |
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)abc.a.实验装置保温、隔热效果差b.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中.
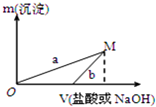 下列两种方案制备氢氧化铝:
下列两种方案制备氢氧化铝:方案一:2.7g Al $\stackrel{100mL稀盐酸}{→}$X溶液 $\stackrel{NaOH溶液}{→}$Al(OH)3沉淀
方案二:2.7g Al $\stackrel{100mLNaOH溶液}{→}$Y溶液$\stackrel{稀盐酸}{→}$Al(OH)3沉淀
已知所用的稀盐酸与NaOH溶液均为3mol/L.图是向X溶液与Y溶液中分别加入NaOH溶液或稀盐酸时产生沉淀的质量与加入溶液体积之间的关系.相关说法正确的是( )
| A. | a曲线表示的是向Y溶液中加入NaOH溶液 | |
| B. | 方案二比方案一生成更多的气体 | |
| C. | 在M点时,两种方案中所得溶液的溶质质量分数相同 | |
| D. | M点以后,a、b两条曲线将重合为一条 |
| A. | pH=3的NH4Cl溶液与pH=3的盐酸中,水电离的c(H+)相等 | |
| B. | 25℃时将0.1 mol•L-1的HF加水不断稀释,$\frac{c({H}^{+})•c({F}^{-})}{c(HF)}$减小 | |
| C. | K2SO3溶液中加入少量的Ba(OH)2固体,溶液的pH增大,SO${\;}_{3}^{2-}$水解程度减小 | |
| D. | 因为AgBr比AgCl的KSP小,所以AgCl可以转化为AgBr,但AgBr无法转化为AgCl |