题目内容
【题目】已知 X、Y 和 Z 三种元素的原子序数之和等于 42。X 元素原子的 4p 轨道上有 3 个未成对电子,Y 元素原子的最外层 2p 轨道上有 2 个未成对电子。X 与 Y 可形成化合物X2Y3 ,Z 元素可形成负一价离子。下列说法正确的是( )
A.X 元素基态原子的电子排布式为[Ar]4s2 4p3
B.X 元素是第 4 周期第 VA 族元素
C.Z 元素的单质在氧气中不能燃烧
D.Y 元素基态原子的轨道表示式为
【答案】B
【解析】
X元素原子的4p轨道上有3个未成对电子,X元素原子的核外电子排布式为1s22s22p63s23p63d104s24p3,处于第四周期第ⅤA族,故X为As元素;Y元素原子的最外层2p轨道上有2个未成对电子,Y的2p轨道上有2个电子或4个电子,所以Y为碳元素或氧元素,X跟Y可形成化合物X2Y3,故Y为氧元素;X、Y和Z三种元素的原子序数之和等于42,则Z的质子数为42-8-33=1,则Z为氢元素,氢原子可以形成负一价离子,符合题意,据此解答。
A.X元素原子的4p轨道上有3个未成对电子,原子的核外电子排布式为1s22s22p63s23p63d104s24p3或[Ar]3d104s2 4p3,故A错误;
B.X原子的核外电子排布式为1s22s22p63s23p63d104s24p3,X为As元素,处于第四周期第ⅤA族,故B正确;
C.Z为氢元素,氢气在氧气中能燃烧,故C错误;
D.Y为O元素,O元素为8号元素,原子核外有8个电子,所以核外电子排布式为:1s22s22p4,基态原子的轨道表示式为![]() ,故D错误;
,故D错误;
答案选B。

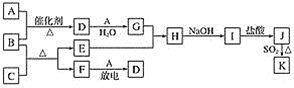
【题目】1,2-二溴乙烷可作汽油抗爆剂的添加剂,在实验室中可以用下图所示装置制备1,2-二溴乙烷.其中 A 和 F 中装有乙醇和浓硫酸的混合液,D 中的试管里装有液溴。A 中可能存在的副反应有:①乙醇在浓硫酸的存在下在 l40℃脱水生成乙醚。②温度过高产生 CO2(夹持装置已略去)
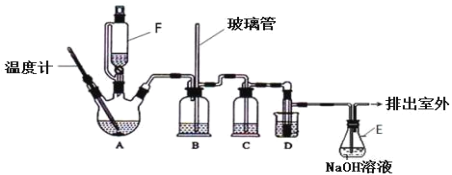
有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g· cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -130 | 9 | -116 |
填写下列空白:
(1)A 中发生的主反应的化学方程式:_____;
(2)D 中发生反应的化学方程式为:_____。
(3)安全瓶 B 可以防止倒吸,并可以检查实验进行时导管是否发生堵塞.请写出发生堵塞时瓶 B 中的现象_____。
(4)在装置 C 中应加入_____,其目的是吸收反应中可能生成的酸性气体。
a 水 b 浓硫酸 c 氢氧化钠溶液 d 饱和碳酸氢钠溶液
(5)容器 E 中 NaOH 溶液的作用是_____。
(6)若产物中有少量副产物乙醚,可用_____(填操作名称)的方法除去。
【题目】如图所示是酸雨的形成示意图。根据图示回答下列问题。
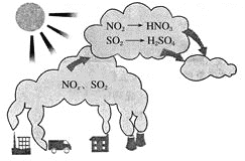
(1)下列气体容易形成酸雨的是_____。
A.CO2 B.SO2 C.N2 D.NO2
(2)现有雨水样品1份,每隔一段时间测定该雨水样品的pH,所得数据如下:
测试时间/h | 0 | 1 | 2 | 3 | 4 |
与水的pH | 4.73 | 4.63 | 4.56 | 4.55 | 4.55 |
分析数据,回答下列问题:
①雨水样品的pH变化的原因是____(用化学方程式表示)。
②如果将刚取样的上述雨水和自来水相混合,pH将变____,原因是_____(用化学方程式表示)。
(3)下列措施中,可减少酸雨产生的途径的是____(填字母)。
①少用煤作燃料 ②把工厂烟囱造高 ③燃料脱硫 ④在已酸化的土壤中加石灰 ⑤开发新能源
A.①②③ B.②③④⑤ C.①③⑤ D.①③④⑤