题目内容
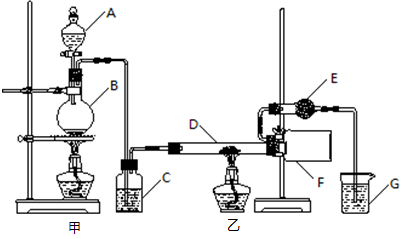
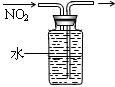
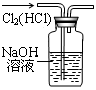
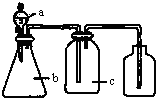
氧化二氯是棕黄色刺激性气体,熔点:﹣116℃,沸点3.8℃.氧化二氯不稳定,接触一般有机物易爆炸;它易溶于水(1:100),同时反应生成次氯酸溶液;制备出之后要冷却成固态以便操作和贮存.制备少量Cl2O,是用干燥的氯气和HgO反应(还生成HgO?HgCl2).装置示意如图(铁架台和夹持仪器已略去).
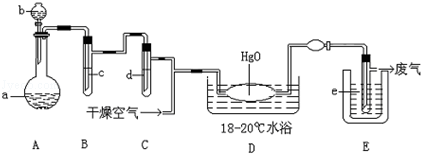
(1)A中盛有的深色固体试剂a是 ,分液漏斗中试剂b是
(2)B中盛有液体c是 ,C中的液体d是
(3)D中所发生反应的化学方程式是
(4)E中的保温瓶中盛有致冷剂,它应是 (在干冰、冰水、液态空气中选择),在E的内管得到的氧化二氯中可能含有杂质是
(5)装置A、B、C间的连接方式与D、E间的连接方式有明显的区别,这区别是 ,用这些不同的连接方式的主要理由是 .

(1)A中盛有的深色固体试剂a是 ,分液漏斗中试剂b是
(2)B中盛有液体c是 ,C中的液体d是
(3)D中所发生反应的化学方程式是
(4)E中的保温瓶中盛有致冷剂,它应是 (在干冰、冰水、液态空气中选择),在E的内管得到的氧化二氯中可能含有杂质是
(5)装置A、B、C间的连接方式与D、E间的连接方式有明显的区别,这区别是 ,用这些不同的连接方式的主要理由是 .
(1)高锰酸钾;浓盐酸.(2)饱和食盐水;浓硫酸.(3)2HgO+2Cl2=Cl2O+HgO?HgCl2.
(4)液态空气;液氯.(5)A、B、C间用乳胶管连接,D、E间不能乳胶管连接;Cl2O遇有机物易爆炸.
(4)液态空气;液氯.(5)A、B、C间用乳胶管连接,D、E间不能乳胶管连接;Cl2O遇有机物易爆炸.
试题分析:(1)由装置图可知,A中发生反应制备氯气,反应不需加热,深色固体试剂a与溶液b反应,通常应为高锰酸钾与浓盐酸,故a为高锰酸钾,b为浓盐酸.故答案为:高锰酸钾;浓盐酸.(2)HCl易挥发,A中生成的氯气中含有HCl、H2O,用饱和食盐水吸收HCl,用浓硫酸干燥,先除氯化氢,后干燥.故B中盛有液体c是试剂饱和食盐水,C中的液体d是浓硫酸.故答案为:饱和食盐水;浓硫酸.(3)由信息可知,D中氯气与HgO反应生成Cl2O与HgO?HgCl2.反应方程式为2HgO+2Cl2=Cl2O+HgO?HgCl2.故答案为:2HgO+2Cl2=Cl2O+HgO?HgCl2.(4)由题目信息可知,氧化二氯气体的熔点﹣116℃,熔点很低.所以选择沸点很低的液态空气进行制冷.根据工艺流程可知,D中反应氯气可能不能成分反应,由于氯气易液化,所以E的内管得到的氧化二氯中可能含有杂质是液氯.故答案为:液态空气;液氯.(5)由信息可知,氧化二氯不稳定,接触一般有机物易爆炸,因此 Cl2O不能与有机物接触,所以A、B、C间用乳胶管连接,D、E间不能乳胶管连接.故答案为:A、B、C间用乳胶管连接,D、E间不能乳胶管连接;Cl2O遇有机物易爆炸.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
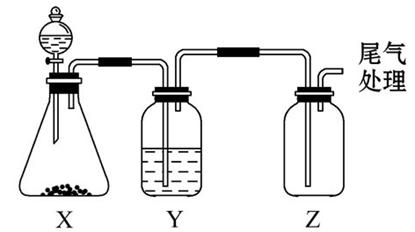
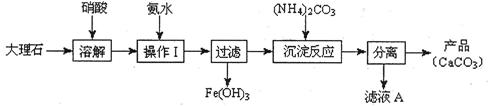
 2CaO+2S02↑+O2↑。
2CaO+2S02↑+O2↑。