题目内容
9.下列能大量共存的离子组是( )| A. | K+、Ba2+、NO3-、HCO3- | B. | Fe2+、H+、Cl-、NO3- | ||
| C. | K+、NH4+、SO42-、OH- | D. | H+、Na+、CO32-、SO42- |
分析 根据离子之间不能结合生成水、气体、沉淀、弱电解质等,不能发生氧化还原反应等,则离子大量共存,以此来解答.
解答 解:A.该组离子之间不反应,可大量共存,故A正确;
B.Fe2+、H+、NO3-发生氧化还原反应,不能大量共存,故B错误;
C.NH4+、OH-结合生成弱电解质,不能大量共存,故C错误;
D.H+、CO32-结合生成水和气体,不能大量共存,故D错误;
故选A.
点评 本题考查离子的共存,为高频考点,把握常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应及分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
19.下列实验能达到预期目的是( )
| A. | 可以用热的浓NaOH溶液来区分植物油和矿物油 | |
| B. | 向经唾液充分作用后的米饭中滴入碘水检验出有淀粉 | |
| C. | 将纤维素和稀H2SO4加热水解后的液体取出少许,加入新制的Cu(OH)2并加热,有砖红色沉淀生成,证明水解生成了葡萄糖 | |
| D. | 蛋白质溶液中加入乙醇可以使蛋白质从溶液中析出,再加水又能溶解 |
17.下列反应中属于氧化还原反应的是( )
| A. | SO2+H2O═H2SO3 | B. | 2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑ | ||
| C. | 2FeCl2+Cl2═2FeCl3 | D. | Al(OH)3+3HCl═AlCl3+3H2O |
14.下列说法不正确的是 ( )
| A. | 过滤分离和提纯物质方法是根据物质颗粒大小的差别 | |
| B. | 对液态混合物可以利用各组分的沸点不同用蒸馏的方法除去易挥发、难挥发或不挥发的杂质 | |
| C. | 用四氯化碳萃取碘的饱和水溶液中的碘,分液时显紫红色液体在上层 | |
| D. | 不慎将油汤洒在衣服上可用酒精、汽油除去 |
1.已知NA为阿伏加德罗常数的值,下列叙述不正确的是( )
| A. | 常温常压下,1mol苯分子中含有碳氢单键数为6NA | |
| B. | 52g C2H2中含有的共用电子对数为10NA | |
| C. | 标准状况下,2.24 L乙烯和丙烯混合气体中含有5NA氢原子 | |
| D. | 标准状况下,2.24 L溴乙烷中含溴原子数目大于0.1NA |
18.下列反应中属于氧化还原反应的是( )
| A. | CO2+2NaOH═Na2CO3+H2O | B. | CuO+2HCl═CuCl2+H2O | ||
| C. | CaCO3+2HCl═CaCl2+H2O+CO2↑ | D. | CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO |
19.下列装置或操作能达到实验目的是( )
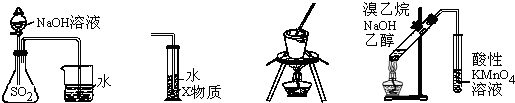

| A. | 装置①可用于证明SO2与NaOH溶液发生了反应 | |
| B. | 装置②中X为CCl4,可用于吸收氨气或氯化氢 | |
| C. | 装置③可用于实验室从食盐水中提取氯化钠 | |
| D. | 装置④可用于证明溴乙烷与NaOH醇溶液共热生成乙烯 |