题目内容
(12分)将碱溶液A、盐溶液B按如下程度进行实验,根据下述现象判断:
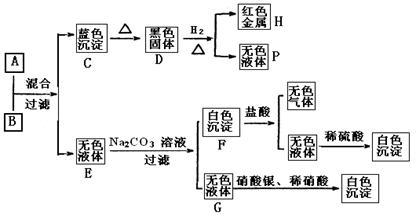
(1)A的化学式 B的化学式 。
(2)完成下列转化的化学方程式,并用“单线桥法”标明电子转移的方向和数目:
D→H+P:
(3) 写出下列反应的离子方程式:
A+B:
F+盐酸:
(4)盐溶液B中阴离子的检验方法是

(1)A的化学式 B的化学式 。
(2)完成下列转化的化学方程式,并用“单线桥法”标明电子转移的方向和数目:
D→H+P:
(3) 写出下列反应的离子方程式:
A+B:
F+盐酸:
(4)盐溶液B中阴离子的检验方法是
(1) Ba(OH)2 (2分) CuCl2 (2分)
 (2)D→H+P: CuO+H2 Cu+H2O (2分)
(2)D→H+P: CuO+H2 Cu+H2O (2分)
(3) 离子方程式:
A+B: Cu2++2OH-=Cu(OH)2↓ (2分)
F+盐酸: Ba CO3+2H+=Ba 2++CO2↑+H2O (2分)
(4)取少量A溶液于试管中,滴加硝酸银溶液产生白色沉淀,再滴加稀硝酸沉淀不溶解。(2分)
 |
 (2)D→H+P: CuO+H2 Cu+H2O (2分)
(2)D→H+P: CuO+H2 Cu+H2O (2分)(3) 离子方程式:
A+B: Cu2++2OH-=Cu(OH)2↓ (2分)
F+盐酸: Ba CO3+2H+=Ba 2++CO2↑+H2O (2分)
(4)取少量A溶液于试管中,滴加硝酸银溶液产生白色沉淀,再滴加稀硝酸沉淀不溶解。(2分)
略

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目
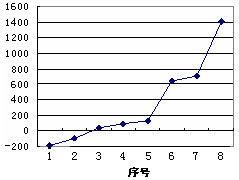
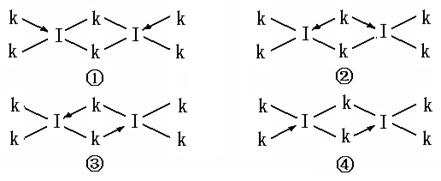

 设计一个实验,不用实验室里的任何试剂,只用常用的仪器,区分B、Y两种物质(简要说明实验方法和实验结论)
设计一个实验,不用实验室里的任何试剂,只用常用的仪器,区分B、Y两种物质(简要说明实验方法和实验结论)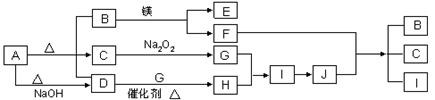

 (A-N+m)mol
(A-N+m)mol (A-N)mol
(A-N)mol  (A-N)mol
(A-N)mol  和
和 为不同的核素,二者核外电子数不同
为不同的核素,二者核外电子数不同