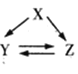题目内容
【题目】0.1 mol/L二元弱酸H2A溶液中滴加0.1mol/LNaOH溶液,溶液中的H2A、HA-、A2 -的物质的量分数δ(x)随pH的变化如图所示。下列说法错误的是

A.pH =1.9时,c(Na+)<c(HA-)+2c(A2-)
B.当c(Na+)=c(H2A)+c(HA-)+c(A2-)时,溶液pH>7
C.pH=6时,c(Na+)>c(HA-)>c(A2-)>c(H2A)
D.lg[Ka2(H2A)]=-7.2
【答案】B
【解析】
A.根据图像,pH =1.9时,溶液显酸性,c(H+)>c(OH-),根据电荷守恒,有c(Na+)+ c(H+)=c(HA-)+2c(A2-)+ c(OH-),因此c(Na+)<c(HA-)+2c(A2-),故A正确;
B.根据图像,当溶液中的溶质为NaHA,溶液显酸性,pH<7,此时溶液中存在物料守恒,c(Na+)=c(H2A)+c(HA-)+c(A2-),故B错误;
C.根据图像,pH=6时,c(HA-)>c(A2-),溶液中的溶质为NaHA和Na2A,c(Na+)>c(HA-)>c(A2一)>c(H2A),故C正确;
D.Ka2(H2A)=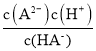 ,根据图像,当pH=7.2时,c(HA-)=c(A2一),则Ka2(H2A)=
,根据图像,当pH=7.2时,c(HA-)=c(A2一),则Ka2(H2A)=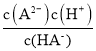 = c(H+)=10-7.2,因此lg[Ka2(H2A)]=-7.2,故D正确;
= c(H+)=10-7.2,因此lg[Ka2(H2A)]=-7.2,故D正确;
故选B。

 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案【题目】下表各组物质(或者它们的溶液)通过一步反应可实现如图所示的转化的是
选项 | X | Y | Z |
|
A | Si | Na2SiO3 | H2SiO3 | |
B | S | H2S | SO2 | |
C | Al2O3 | NaAlO2 | Al2(SO4)3 | |
D | Mg(OH)2 | MgCO3 | MgCl2 |
A.AB.BC.CD.D
【题目】二氧化碳的回收利用对温室气体的减排具有重要的意义。在2L密闭容器中,加入2.00molCO2和2.0 mol H2以及催化剂发生反应:CO2(g)+H2 (g)![]() HCOOH(g) ΔH,测得,n(H2)/mol在不同温度随时间的变化如下表:
HCOOH(g) ΔH,测得,n(H2)/mol在不同温度随时间的变化如下表:
60 min | 90 min | 120 min | 150 min | 180 min | ||
实验I | Tl/K | 1.50 mol | 1.32 mol | 1.28 mol | 1.26 mol | 1.26 mol |
实验Ⅱ | T2/K | 1.45 mol | 1.20 mol | 1.10 mol | 1.10 mol | 1.10 mol |
(1)比较实验温度T1___T2(填“>”、“<”),该反应的ΔH___0(填“>”、“=”、“<”)。
(2)实验I中0~60 min内用HCOOH表示的该反应的平均反应速率为_____。
(3)实验Ⅱ反应开始时体系压强为P0,第90min时体系压强为Pl,则Pl∶P0=___。
(4)比较实验I、Ⅱ在80min时的逆反应速率大小vl___vⅡ(填“>”、“<”或“无法判断”),原因是_____。