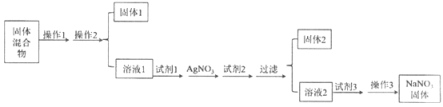
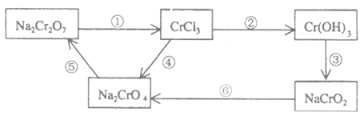
题目内容
【题目】如下图所示操作能实现实验目的的是( )
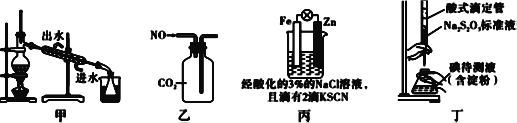
A. 用图甲装置分离碘和四氯化碳,在锥形瓶中收集到碘单质
B. 用图乙装置收集NO气体
C. 用图丙装置验证牺牲阳极的阴极保护法
D. 用图丁装置测定待测液中I2的含量
【答案】B
【解析】A. 用图甲装置分离碘和四氯化碳,在锥形瓶中收集到四氯化碳,选项A错误;B. NO遇空气能与氧气反应,不能排空气法收集,但密度比二氧化碳小且不反应,可用图乙装置收集NO气体,选项B正确;C、原电池锌做负极失电子发生氧化反应,铁做正极被保护,检验亚铁离子生成的试剂铁氰酸钾而不应用KSCN,所以装置不能验证牺牲阳极的阴极保护法,选项C错误;D、硫代硫酸钠呈碱性,必须装在碱式滴定管,选项D错误。答案选B。

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目