题目内容
【题目】不能证明CH3COOH是弱电解质的实验事实是( )
A. CH3COONa溶液显碱性
B. 0.1mol/LCH3COOH溶液pH>1
C. 用CH3COOH溶液浸泡水壶中的水垢,可将其清除
D. 25℃时,0.1mo/LCH3COOH溶液比0.1mol/LHCl溶液导电性弱
【答案】C
【解析】A,CH3COONa溶液显碱性说明CH3COO-发生了水解,说明CH3COOH是弱酸;B,0.1mol/LCH3COOH溶液的pH![]() 1,溶液中c(H+)
1,溶液中c(H+)![]() 0.1mol/L,说明CH3COOH部分发生电离,CH3COOH是弱酸;C,用CH3COOH溶液浸泡水壶中的水垢发生反应2CH3COOH+CaCO3=(CH3COO)2Ca+H2O+CO2↑,说明酸性:CH3COOH
0.1mol/L,说明CH3COOH部分发生电离,CH3COOH是弱酸;C,用CH3COOH溶液浸泡水壶中的水垢发生反应2CH3COOH+CaCO3=(CH3COO)2Ca+H2O+CO2↑,说明酸性:CH3COOH![]() H2CO3,不能说明CH3COOH为弱酸;D,25℃时,0.1mol/LCH3COOH溶液比0.1mol/LHCl溶液导电性弱,说明CH3COOH溶液中离子物质的量浓度小于HCl溶液中,CH3COOH未完全电离,说明CH3COOH为弱酸;不能证明CH3COOH是弱电解质的实验事实是C,答案选C。
H2CO3,不能说明CH3COOH为弱酸;D,25℃时,0.1mol/LCH3COOH溶液比0.1mol/LHCl溶液导电性弱,说明CH3COOH溶液中离子物质的量浓度小于HCl溶液中,CH3COOH未完全电离,说明CH3COOH为弱酸;不能证明CH3COOH是弱电解质的实验事实是C,答案选C。

 步步高达标卷系列答案
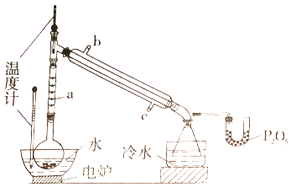
步步高达标卷系列答案【题目】硼酸三甲酯用作柠檬类水果的熏蒸剂。实验室合成硼酸三甲酯的原理及装置如下:
硼酸三甲酯 | 甲醇 | |
溶解性 | 与乙醚、甲醇混溶,能水解 | 与水混溶 |
沸点/℃ | 68 | 64 |
硼酸三甲酯与甲醇混合物的共沸点为54℃ | ||
Na2B4O7·10H2O+2H2SO4+16CH3OH![]() 2NaHSO4+4[(CH3O)3B+CH3OH]+17H2O
2NaHSO4+4[(CH3O)3B+CH3OH]+17H2O
实验步骤如下:
①在圆底烧瓶中加入44.8g甲醇和19.1gNa2B4O7·10H2O (硼砂,式量为382),然后缓慢加入浓H2SO4并振荡;加热烧瓶中的液体;通过分馏柱回流一段时间。
②先接收51~55℃的馏分,再接收55~60℃的馏分。
③将两次馏分合并,加入氯化钙进行盐析分层,上层为硼酸三甲酯,分离。
④精馏得高纯硼酸三甲酯19.2g。
回答下列问题:
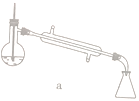
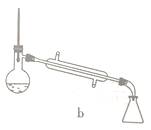
(1)图中仪器a的名称为____________;直形冷凝管冷却水应从____________(填“b”或“c”)接口进入。
(2)本实验加热方式为____________,优点是____________。
(3)加入氯化钙盐析分层的主要目的是____________。
(4)U型管中P2O5的作用是_____________________________________。
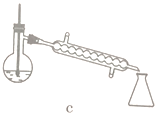
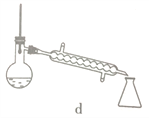
(5)步骤④的仪器选择及安装都正确的是____________ (填标号),应收集____________℃的馏分。
(6)本次实验的产率是____________。
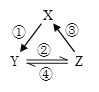
【题目】X、Y、Z 是中学化学中常见的三种物质,下表各组物质之间通过一步反应不能实现右图所示转化关系的是
X | Y | Z | 箭头上所标数字的反应条件 | ||
A. | NO | NO2 | HNO3 | ①常温遇氧气 |
|
B. | Cl2 | NaClO | HClO | ②通入CO2 | |
C. | Na2O2 | NaOH | NaCl | ③加入H2O2 | |
D. | Al2O3 | NaAlO2 | Al(OH)3 | ④加NaOH溶液 |
A. A B. B C. C D. D