题目内容
【题目】下列图示与对应的叙述相符的是
A.图表示反应2SO2 (g)+O2(g)![]() 2SO3 (g) ΔH<0不同温度(T1<T2)时平衡常数K随压强的变化关系图
2SO3 (g) ΔH<0不同温度(T1<T2)时平衡常数K随压强的变化关系图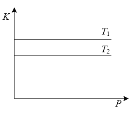
B.图曲线表示电解精炼铜过程中电极质量的变化
C.图曲线表示反应N2(g)+3H2(g)![]() 2NH3(g)在t1时刻增大压强后v(正)、v(逆)随时间的变化
2NH3(g)在t1时刻增大压强后v(正)、v(逆)随时间的变化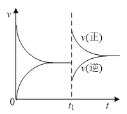
D.图曲线表示0.1000 mol·L—1 NaOH溶液滴定20.00 mL pH=1的CH3COOH溶液所得溶液的pH随NaOH溶液体积的变化
【答案】A
【解析】
A.平衡常数只与温度有关,升温逆向移动,平衡常数减小,故正确;
B. 电解精炼铜时阳极减少,阴极质量增加,但减少部分与增加部分不等,故错误;
C.增大压强正逆反应速率都增大,故错误;
D. 20.00 mL pH=1的CH3COOH溶液中醋酸的浓度大于0.1mol/L,所以中和该醋酸需要的氢氧化钠的体积大于20毫升,所以pH突变时的数据大于20毫升,故错误。
故选A。

练习册系列答案
相关题目