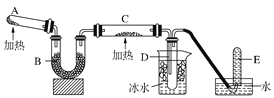
��Ŀ����
����Ŀ��A��B��C��D��E��Ϊ������Ԫ�أ�A�����ԭ��������С��Ԫ�أ�B��+1�������Ӻ�C�ĩ�1�������Ӷ�����ԭ�Ӿ�����ͬ�ĵ��Ӳ�ṹ��D��C����һ���ڣ�����B�γ�BD�����ӻ����E��CΪͬһ����Ԫ�أ�������������Ӧ��ˮ����Ϊһ��ǿ�ᡣ�����������Ϣ�ش��������⣺
��1��BԪ����Ԫ�����ڱ��е�λ���ǵ�______����______�壻
��2������CԪ�ص�ԭ�ӽṹʾ��ͼ______��
��3����E���⻯�������������������ȵķ�����______����һ�����ѧʽ����ͬ������������______��
��4��A��D�γɵĻ������к��л�ѧ����������_____��
���𰸡� �� ��A ![]() H2O �� NH3�� HF �� CH4 Na +�� Mg 2+�� NH4 +�� H3O+ ���Թ��ۼ�
H2O �� NH3�� HF �� CH4 Na +�� Mg 2+�� NH4 +�� H3O+ ���Թ��ۼ�
��������A��B��C��D��E��Ϊ������Ԫ�أ�A�����ԭ��������С�ģ���AΪ��Ԫ�أ�B��+1�������Ӻ�C��-1�������Ӷ�����ԭ�Ӿ�����ͬ�ĵ��Ӳ��Ų�����BΪNaԪ�أ�CΪFԪ�أ�D��C����һ���ڣ�����B�γ�BD�����ӻ������DΪClԪ�أ�E��CΪͬһ����Ԫ�أ�������������ˮ����Ϊǿ�ᣬ��EΪNԪ�أ�
��1��BΪNaԪ�أ��������ڱ��е�������IA�壻
��2��CΪFԪ�أ�ԭ�ӽṹʾ��ͼΪ![]() ��
��
��3��E���⻯�����ΪNH3����֮��������������ȵķ�����H2O�ȣ�������OH-��-��
��4��A��D�γɵĻ�����ΪHCl�����й��ۼ���

 ������������ϵ�д�
������������ϵ�д�����Ŀ����2017�����ʡ��ɳ�г�����ѧ������һ��ģ�⡿
��������Ƶ�����֣�����Ӱ�����ǵ�����ͽ�����������Ҫ��Ⱦ��Ϊ�����������PM2.5������Ҫ��ԴΪȼú��������β���ȡ���ˣ���PM2.5��SO2��NOx�Ƚ����о�������Ҫ���塣��ش��������⣺
��1����PM2.5����������ˮ�����Ƴɴ���������
����ø���������ˮ���������ӵĻ�ѧ��ּ���ƽ��Ũ�����±���
���� | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
Ũ��mol/L | 4��10-6 | 6��10-6 | 2��10-5 | 4��10-5 | 3��10-5 | 2��10-5 |
���ݱ��������ж�������pH=_________��
��2������β����NOx��CO�����ɣ�
����֪����������NO�ķ�ӦΪ��N2(g)+O2(g)![]() 2NO(g) ��H>0���£������ܱ������У�����˵������˵���÷�Ӧ�ﵽ��ѧƽ��״̬����____
2NO(g) ��H>0���£������ܱ������У�����˵������˵���÷�Ӧ�ﵽ��ѧƽ��״̬����____
A.���������ܶȲ��ٱ仯 B.��������ƽ�����������ٱ仯
C.N2��O2��NO�����ʵ���֮��Ϊ1��1��2 D.�����İٷֺ������ٱ仯
������ȼ�Ͳ���ȫȼ��ʱ����CO���������밴���з�Ӧ��ȥCO��2CO(g)=2C(s)+O2(g)����֪�÷�Ӧ����H��0����������ܷ�ʵ��______________����ܡ����ܡ���
��3��Ϊ����SO2���ŷţ�����ȡ�Ĵ�ʩ�У�
����úת��Ϊ�������ȼ�ϡ���֪��
H2(g)+ 1/2O2(g) =H2O(g) ��H=��241.8kJ��mol-1
C(s)+1/2O2(g) =CO(g)��H =-110.5kJ��mol-1
д����̿��ˮ������Ӧ���Ȼ�ѧ����ʽ��___________________��
��ϴ�Ӻ�SO2��������
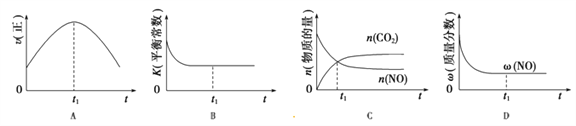
��4������β����������Ҫԭ����2NO(g)+2CO(g)![]() 2CO2(g)+N2(g)����H��0�����÷�Ӧ�ھ��ȡ����ݵ��ܱ���ϵ�н��У�����ʾ��ͼ��ȷ����˵����Ӧ�ڽ��е�t1ʱ�̴ﵽƽ��״̬����_________������ţ�������ͼ��v����K��n��w�ֱ��ʾ����Ӧ���ʡ�ƽ�ⳣ�������ʵ���������������
2CO2(g)+N2(g)����H��0�����÷�Ӧ�ھ��ȡ����ݵ��ܱ���ϵ�н��У�����ʾ��ͼ��ȷ����˵����Ӧ�ڽ��е�t1ʱ�̴ﵽƽ��״̬����_________������ţ�������ͼ��v����K��n��w�ֱ��ʾ����Ӧ���ʡ�ƽ�ⳣ�������ʵ���������������
��5�������ŷŵĵ������úȼ�ղ����Ķ��������ǵ������������ġ�������ס�֮һ������̿�ɴ���������Ⱦ��NO����5L�ܱ������м���NO�ͻ���̿�����������ʣ���һ����������������E��F�����¶ȷֱ���T1����T2��ʱ����ø�����ƽ��ʱ���ʵ�����n/mol�����±���
���� �¶�/�� | ����̿ | NO | E | F |
��ʼ | 3.000 | 0.10 | 0 | 0 |
T1 | 2.960 | 0.020 | 0.040 | 0.040 |
T2 | 2.975 | 0.050 | 0.025 | 0.025 |
�� д��NO�����̿��Ӧ�Ļ�ѧ����ʽ______________________��
������������ӦT1��ʱ��ƽ�ⳣ��K1=__________________����T1��T2����÷�Ӧ����H__________________0(���������������������
�� ������ӦT1��ʱ�ﵽ��ѧƽ�����ͨ��0.1molNO���壬��ﵽ�»�ѧƽ��ʱNO��ת����Ϊ________��