题目内容
【题目】U,W,Y是原子序数依次增大的短周期主族元素,在周期表中的相对位置如右表;U元素与氧元素能形成两种无色气体;W是地壳中含量最多的金属元素.
U | |||
W | Y |
(1)元素U的原子核外共有种不同能级的电子.
(2)能提高W与稀硫酸反应速率的方法是
a.使用浓硫酸 b.加热 c.加压 d.使用等质量的W粉末
(3)在恒容密闭容器中进行:2YO2(g)+O2(g) ![]() 2YO3(g)△H2=﹣190kJ/mol
2YO3(g)△H2=﹣190kJ/mol
①该反应 450℃时的平衡常数500℃时的平衡常数(填<,>或=).
②下列描述中能说明上述反应已达平衡的是
a.2ν(O2)正=ν(YO3)逆 b.气体的平均分子量不随时间而变化
c.反应时气体的密度不随时间而变化 d.反应时气体的分子总数不随时间而变化
③在一个固定容积为2L的密闭容器中充入0.20mol YO2和0.10molO2 , 半分钟后达到平衡,测得容器中含YO30.18mol,则ν(O2)=:平衡常数为 . 若继续通入0.20molYO2和0.10molO2 , 再次达到平衡后,YO3物质的量约为 .
【答案】
(1)3
(2)bd
(3)>;abd;0.09mol/(L.min);16200;0.368mol
【解析】解:U、W、Y是原子序数依次增大的短周期主族元素,W是地壳中含量最多的金属元素,W是Al元素;根据元素在周期表中的位置可知U为C元素、Y为S元素.(1)元素U为碳,原子核外电子排布式为1s22s22p2 , 其原子核外共有1s、2s、2p三种能级电子,所以答案是:3;(2)a.Al在浓硫酸中会发生钝化现象,使用浓硫酸不能加快反应速率,故a错误;
b.升高温度,可以加快反应速率,故b正确;
c.没有气体参加反应,加压不能加快反应速率,故c错误;
d.使用等质量的W粉末,增大接触面积,可以加快反应速率,故d正确,
故选:bd;(3)①正反应放热反应,升高温度平衡逆向移动,平衡常数减小,即450℃时的平衡常数大于500℃时的平衡常数,
所以答案是:>;②a.2ν(O2)正=ν(YO3)逆时,说明YO3正、逆反应速率相等,反应达到平衡状态,故a正确;
b.反应为气体物质的量减小的反应,而气体质量不变,随反应进行平均分子量增大,容器中气体的平均分子量不随时间而变化说明反应达到平衡状态,故b正确;
c.气体总质量不变,恒容密闭容器中气体的密度始终不变,故c错误;
d.反应为气体物质的量减小的反应,容器中气体的分子总数不随时间而变化说明反应达到平衡状态,故d正确,
故选:abd;③半分钟后达到平衡,测得容器中含YO30.18mol,则:
2YO2(g)+O2(g)2YO3(g)
起始(mol):0.2 0.1 0
变化(mol):0.18 0.09 0.18
平衡(mol):0.02 0.01 0.18
故ν(O2)= ![]() =0.09mol/(L.min),
=0.09mol/(L.min),
平衡常数K= ![]() =
= 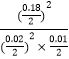 =16200,
=16200,
等效为开始加入0.40molYO2和0.20molO2 , 设平衡时YO3物质的量为x,则:
2YO2(g)+O2(g)2YO3(g)
起始(mol):0.4 0.2 0
变化(mol):x 0.5x x
平衡(mol):0.4﹣x 0.2﹣0.5x x
所以 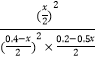 =16200,
=16200,
解得x≈0.368
所以答案是:0.09mol/(L.min);16200;0.368mol.

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案【题目】在恒温条件下起始时容积均为5L的甲、乙两密闭容器中(甲为恒容容器、乙为恒压容器),均进行反应:N2(g)+3H2(g)2NH3(g)△H2=﹣92.4kJ/mol,有关数据及特定平衡状态见表.
容器 | 起始投入 | 达平衡时 | |||
甲 | 2molN2 | 3molH2 | 0molNH3 | 1.5molNH3 | |
乙 | amolN2 | bmolH2 | 0molNH3] | 1.2molNH3 | |
(1)若平衡后同种物质的体积分数相同,起始时乙容器通入的N2的物质的量为 ,
起始时乙中的压强是甲容器的倍,乙的平衡常数为
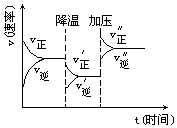
(2)恒容密闭容器中可以发生氨气的分解反应,达平衡后,仅改变下表中反应条件x,下列各项中y随x的增大而增大的是(选填序号).
选项 | a | b | c | d |
x | 温度 | 温度 | 加入H2的物质的量 | 加入氨气的物质的量 |
y | 混合气体的平均相对分子质量 | 平衡常数K | 混合气体的密度 | 达平衡时氨气的转化率 |
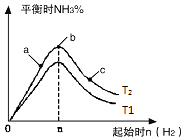
(3)研究在其他条件不变时,改变起始物氢气的物质的量对反应的影响,实验结果如图所示(图中T表示温度,n表示物质的量):
①像中T2和T1的关系是:T2T1(填“高于”“低于”“等于”“无法确定”).
②a、b、c三点中,N2转化率最高的是(填字母).
③若容器容积为1L,T2℃在起始体系中加入1mol N2 , 3molH2 , 经过5min反应达到平衡时H2的转化率为60%,则NH3的反应速率为 . 保持容器体积不变,若起始时向容器内放入2mol N2和6mol H2 , 达平衡后放出的热量为Q,则Q110.88kJ(填“>”、“<”或“=”).