题目内容
11.下列有关化学用语的表达正确的是( )| A. | CO2的比例模型: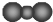 | B. | N原子最外层轨道表示式: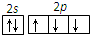 | ||
| C. | Cl原子的结构示意图: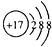 | D. | Al原子最外层电子排布式:3s23p1 |
分析 A.比例模型表示原子的相对大小及原子连接顺序、空间结构;
B.N原子的2p轨道电子的自旋方向应该相同;
C.氯原子的核电荷数=核外电子总数=17,最外层为7个电子;
D.Al原子最外层含有3个电子,结合构造原理写出其最外层电子排布式.
解答 解:A.碳原子半径比氧原子半径大,但比例模型中C原子的比较比O原子半径小,则二氧化碳正确的比例模型为: ,故A错误;
,故A错误;
B.氮原子最外层5个电子,2p轨道的3个电子的自旋方向应该相同,其最外层轨道正确的表示式为: ,故B错误;
,故B错误;
C.氯原子的核电荷数、核外电子总数都是17,最外层只有7个电子,其正确的原子结构示意图为: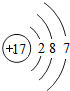 ,故C错误;
,故C错误;
D.Al原子的原子序数为13,最外层含有3个电子,其原子最外层电子排布式:3s23p1,故D正确;
故选D.
点评 本题考查了常见化学用语的表示方法判断,题目难度中等,注意掌握比例模型、轨道排布图、电子排布式、原子结构示意图等化学用语的书写原则,试题培养了学生规范答题的能力.

练习册系列答案
相关题目
2.下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白(填写序号不得分):
(1)⑦元素的离子半径<S2-(填“>”或“<”)写出⑩元素在周期表的位置第四周期ⅦA族;在这些元素中,化学性质最不活泼的是:Ar.(填元素符号)比较③与⑥的氢化物,H2O更稳定(填化学式)
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是HClO4,碱性最强的化合物的化学式是:KOH.
(3)比较①与⑤的最高价氧化物对应的水化物,H2CO3的酸性强(填化学式);用相应的化学方程式证明Na2SiO3+CO2+H2O=H2SiO3↓+Na2CO3.
(4)实验室制取②的氢化物的化学方程式2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;②的最高价氧化物的水化物浓溶液与①的单质反应的化学方程式为:C+4HNO3(浓) $\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+NO2↑+2H2O(用化学方程式表示)
(5)写出④的单质与水反应的离子方程式2Na+2H2O=2Na++2OH-+H2↑.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是HClO4,碱性最强的化合物的化学式是:KOH.
(3)比较①与⑤的最高价氧化物对应的水化物,H2CO3的酸性强(填化学式);用相应的化学方程式证明Na2SiO3+CO2+H2O=H2SiO3↓+Na2CO3.
(4)实验室制取②的氢化物的化学方程式2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;②的最高价氧化物的水化物浓溶液与①的单质反应的化学方程式为:C+4HNO3(浓) $\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+NO2↑+2H2O(用化学方程式表示)
(5)写出④的单质与水反应的离子方程式2Na+2H2O=2Na++2OH-+H2↑.
6.化学与生活密切相关,下列说法正确的是( )
| A. | 铝制容器可长期盛放酸性或碱性物质 | |
| B. | 甲烷会导致某些温泉有臭鸡蛋气味 | |
| C. | 太阳能的开发利用可降低碳排放量 | |
| D. | 塑料垃圾会造成水体富营养化 |
16.已知aq表示溶液状态.
①H+(aq)+OH-(aq)→H2O(l)+a kJ
②NH4+(aq)+H2O(l)H+(aq)+NH3•H2O(aq)+b kJ
③HAc(aq)+OH-(aq)→Ac-(aq)+H2O(l)+c kJ
则a、b、c的大小关系为( )
①H+(aq)+OH-(aq)→H2O(l)+a kJ
②NH4+(aq)+H2O(l)H+(aq)+NH3•H2O(aq)+b kJ
③HAc(aq)+OH-(aq)→Ac-(aq)+H2O(l)+c kJ
则a、b、c的大小关系为( )
| A. | a>c>b | B. | a=b=c | C. | a=c>b | D. | a>c=b |
1.某有机物X的结构简式如图所示,则下列有关说法中正确的是( )


| A. | X的分子式为C5H10O2,该产物属于羧酸的同分异构体有5种 | |
| B. | X在一定条件下能发生加成、加聚、取代、消去等反应 | |
| C. | 在Ni作催化剂的条件下,1 mol X最多只能与1 mol H2加成 | |
| D. | 可用酸性高锰酸钾溶液区分苯和X |
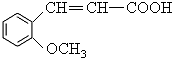 .
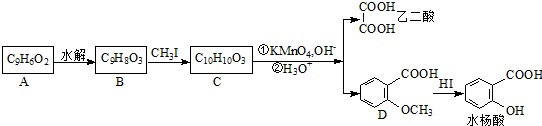
.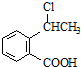 可以最终合成芳香内酯A,其中前两步的反应是
可以最终合成芳香内酯A,其中前两步的反应是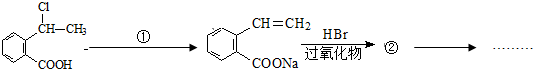
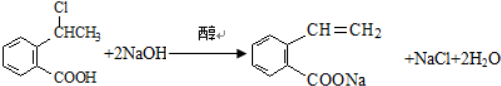 ,产物②的结构简式是
,产物②的结构简式是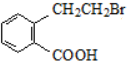 .
.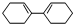 c.
c.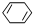 d.
d.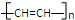
 +
+ $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$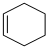 则要制备
则要制备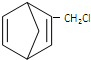 ,含共轭结构的原料可以是
,含共轭结构的原料可以是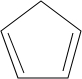 或
或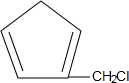 .(写结构简式)
.(写结构简式)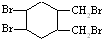 的合成路线(其他无机试剂任选).
的合成路线(其他无机试剂任选).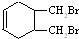 $\stackrel{Br_{2}}{→}$
$\stackrel{Br_{2}}{→}$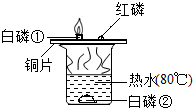 燃烧是我们非常熟悉的化学反应.
燃烧是我们非常熟悉的化学反应.