题目内容
【题目】下列说法正确的是
A.原子核外电子排布式为1s2的原子与原子核外电子排布式为1s22s2的原子化学性质相似
B.Fe3+的最外层电子排布式为3s23p63d5
C.基态铜原子价电子的轨道表示式: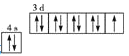
D.基态碳原子价电子的轨道表示式: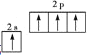
【答案】B
【解析】
A.原子核外电子排布式为1s2的原子是He原子;原子核外电子排布式为1s22s2的原子是Be原子,He是0族元素,Be是第IIA的元素,二者化学性质不相似,A错误;
B.Fe是26号元素,原子核外有26个电子,Fe原子失去最外层2个电子和倒数第二层1个电子形成Fe3+,根据构造原理可知Fe3+最外层电子排布式为3s23p63d5,B正确;
C.Cu是29号元素,根据构造原理,结合泡利不相容原理和洪特规则可知基态Cu原子的价电子排布式是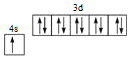 ,C错误;
,C错误;
D.C是6号元素,根据构造原理可得基态碳原子价电子的轨道表示式为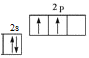 ,D错误;
,D错误;
故合理选项是B。

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
【题目】对下列实验事实的理论解释错误的是( )
选项 | 实验事实 | 理论解释 |
A | 酸性:H2SO4>H2SO3 | H2SO4非羟基氧原子个数大于H2SO3,中心原子正电性越高,酸性越强 |
B | Be单质能溶于KOH溶液 | Be和Al在周期表中是对角线关系,性质相似 |
C | Al原子的第一电离能大于Mg原子 | Mg的金属性比Al强,更容易失去电子 |
D | 沸点:对羟基苯甲醛>邻羟基苯甲醛 | 对羟基苯甲醛存在分子间氢键,邻羟基苯甲醛存在分子内氢键,分子间氢键对它们沸点的影响大于分子内氢键对它们沸点的影响 |
A.AB.BC.CD.D