题目内容
【题目】根据如图所示的转化关系以及现象回答下列问题。
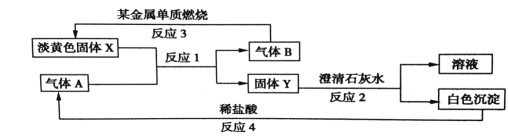
(1)固体 X的化学式是:________________
(2)写出反应1 的化学方程式:____________________________
(3)写出反应2 的离子方程式:________________________________
(4)若15.6gX 和足量的气体 A反应,转移__________mol 电子。
【答案】(1)过氧化钠 Na2CO3(2)2Na2O2+2CO2=2Na2CO3+O2(3)Na2CO3+Ca(OH)2= CaCO3↓+2NaOH(4)0.2
【解析】
试题(1)Na2CO3能与水及二氧化碳发生反应,所以与它反应的气体A是二氧化碳。(2)反应产生碳酸钠和氧气。固体Y是碳酸钠,气体B是氧气。钠在氧气中燃烧得到过氧化钠淡黄色固体。反应的方程式:2Na2O2+2CO2=2Na2CO3+O2。(3)二氧化碳与氢氧化钙发生反应产生碳酸钙沉淀和水。反应的方程式为:Na2CO3+Ca(OH)2= CaCO3↓+2NaOH。碳酸钙与盐酸发生反应生成氯化钙、水和二氧化碳。(4)Na2O2化学式的式量是78,15.6g过氧化钠的物质的量是0.2mol.根据化学方程式:2Na2O2+2H2O=4NaOH+O2↑可知若有2mol过氧化钠反应,转移电子2mol.现在有0.2mol发生反应,所以转移电子0.2mol.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目