题目内容
在短周期中,R原子最外层电子数是其次外层电子数的3倍,下列说法不正确的是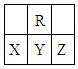
| A.原子半径大小:X >Y>Z |
| B.氢化物的稳定性:X >Y |
| C.化合物YR2能使品红溶液褪色 |
| D.X、Y、Z三种元素最高价氧化物的水化物的酸性最强的是Z |
B
解析试题分析:在短周期中,R原子最外层电子数是其次外层电子数的3倍,则次外层电子数是2个电子,最外层是6个电子,所以R元素是O元素,所以X是P,Y是S,Z是Cl。A、根据元素周期律中原子半径的大小规律,同周期中原子半径岁原子序数的增大而减小,所以原子半径大小:X >Y>Z ,正确;B、元素的非金属性在同周期中岁原子序数的增大而增强,氢化物的稳定性随之而增强,所以氢化物的稳定性:X <Y,错误;C、二氧化硫可使品红溶液褪色,正确;D、X、Y、Z三种元素非金属性最强的是Z,所以最高价氧化物的水化物的酸性最强的是Z,正确,答案选B。
考点:考查元素的推断和元素周期律的应用

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
A、B、C、D是原子序数依次增大的短周期主族元素,A、C在元素周期表中的相对位置如图,A元素最外层与次外层上的电子数之差为3,B为地壳中含最最多的金属元素。
| A | |
| | C |
(1)D原子结构示意图为_____________。
(2)将C的低价态氧化物甲通入到D单质的水溶液会使之褪色,体现了甲的________性,写出该反应的离子方程式_____________________。
(3)A的最高价氧化物对应的水化物是乙,现将过量Cu加入到100 mL 8.0 mol/L乙的浓溶液中,充分反应,共收集到6.72L(标准状况)气体,则该气体的成分是_______________,还原剂失电子数为_________________。
(4)将两份足量的B单质分别加入到等体积等浓度的盐酸和NaOH溶液中,充分反应生成气体的体积比为____________________,若将反应后所得的溶液混合,会生成白色沉淀,发生反应的离子方程式为___________________________________________________;B单质表面的氧化膜可用NaOH溶液除去,写出该反应的化学方程式____________________________________________________________。
W、X、Y、Z四种短周期主族元素的原子序数依次增大,W、X原子的最外层电子数之比为4:3,Z原子比X原子的核外电子数多4。下列说法正确的是
| A.W、Y、Z的电负性大小顺序一定是Z>Y>W |
| B.W、X、Y、Z的原子半径大小顺序可能是W>X>Y>Z |
| C.Y、Z形成的分子的空间构型可能是正四面体 |
| D.WY2分子中δ键与π键的数目之比是2:1 |
下列物质中,S元素的化合价为+6的是
| A.S | B.H2SO4 | C.SO2 | D.H2S |
某元素最高价含氧酸的化学式是H2RO4,该元素的气态氢化物化学式可表示为
| A.HR | B.H2R | C.RH3 | D.不能确定 |
下列微粒:①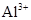 ;②
;② ;③
;③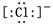 ;④
;④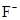 。其中核外电子数相同的是( )
。其中核外电子数相同的是( )
| A.①②③ | B.②③④ | C.①②④ | D.①③④ |
下列有关物质性质的说法错误的是
| A.热稳定性:HCl> HI | B.原子半径:Na> Mg |
| C.结合质子能力:S2-> Cl- | D.酸性:H2SO3>H2SO4 |
下列说法正确的是( )
| A.形成离子键的阴阳离子间只存在静电吸引力 |
| B.HF、HCl、HBr、HI的热稳定性和还原性从左到右依次减弱 |
| C.第三周期非金属元素含氧酸的酸性从左到右依次增强 |
| D.元素周期律是元素原子核外电子排布周期性变化的结果 |
a、b、c、d是四种短周期元素。a、b、d同周期,c、d同主族。a的原子结构示意图为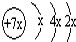 ,b与c形成化合物的电子式为
,b与c形成化合物的电子式为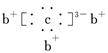 ,下列比较中正确的是( )
,下列比较中正确的是( )
| A.原子半径:a>c>d>b | B.最高价氧化物对应水化物的酸性:c>d>a |
| C.原子序数:a>d>b>c | D.单质的氧化性:a>b>d>c |