题目内容
1mol MnO2与含4mol HCl的浓盐酸共热,在不考虑HCl挥发的情况下得到氯气为( )
| A、2mol |
| B、1mol |
| C、小于1mol |
| D、大于2mol |
考点:氯、溴、碘及其化合物的综合应用
专题:卤族元素
分析:MnO2与浓HCl反应,随着反应的进行,浓HCl变稀,稀盐酸不能与MnO2反应,以此解答.
解答:
解:实验室制取氯气的化学方程式为MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,MnO2不能氧化稀盐酸,
随着反应的进行,浓HCl变稀,稀盐酸不能与MnO2反应,MnO2足量时,不能准确计算出氯气的量,故反应中产生的氯气小于1mol.
故选C.
| ||
随着反应的进行,浓HCl变稀,稀盐酸不能与MnO2反应,MnO2足量时,不能准确计算出氯气的量,故反应中产生的氯气小于1mol.
故选C.
点评:本题考查氯气的制备,题目难度不大,注意氯气的实验室制法以及浓稀盐酸的性质的差异性,注意稀盐酸与二氧化锰不反应.

练习册系列答案
相关题目
分别测得反应2SO2+O2
2SO3的速率如下,其中最快的是( )
| ||
| △ |
| A、v(SO2)=4 mol/(L?min) |
| B、v(O2)=3 mol/(L?min) |
| C、v(SO2)=0.1 mol/(L?s) |
| D、v(O2)=0.1 mol/(L?s) |
下列试剂中,能用于检验酒精中是否含有水的是( )
| A、CuSO4?5H2O |
| B、CuSO4 |
| C、金属钠 |
| D、浓硫酸 |
下列有关阴离子的说法正确的是( )
①阴离子一定是酸根离子
②只有活泼的非金属元素才能形成阴离子
③阴离子中不能含有金属元素
④C、Si等第ⅣA族元素的原子很难得电子也就难形成简单阴离子.
①阴离子一定是酸根离子
②只有活泼的非金属元素才能形成阴离子
③阴离子中不能含有金属元素
④C、Si等第ⅣA族元素的原子很难得电子也就难形成简单阴离子.
| A、①②③④ | B、①④ |
| C、①②④ | D、④ |
下列物质水解时,最难断裂的化学键是( )
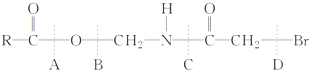
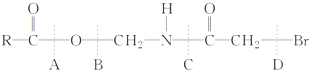
| A、A | B、B | C、C | D、D |
0.1mol/L KHSO4和0.1mol/L Na2S溶液等体积混合后,溶液能使pH试纸变蓝,则离子浓度关系不正确的是( )
| A、c(SO42-)>c(HS-)>c(OH-)>c(H+) |
| B、c(Na+)=c(S2-)+c(H2S)+c(HS-)+c(SO42-) |
| C、c(Na+)+c(K+)+c(H+)=2c(SO42-)+2c(S2-)+c(HS-)+c(OH-) |
| D、c(Na+)>c(K+)>c(H+)>c(OH-) |
下列叙述中,不正确的是( )
| A、硅和锗都是重要的半导体材料 |
| B、地壳中含量占第一、二位两种元素组成的一种化合物为SiO2 |
| C、自然界里存在大量的单质硅、二氧化硅和硅酸盐 |
| D、常温下硅的化学性质不活泼,不易与氧气,氢气,氯气发生化学反应 |
下列物质属于非电解质且溶于水能导电的是( )
| A、Na |
| B、H2S |
| C、Cl2 |
| D、NH3 |